Mik azok az intrauterin fertőzések? A húgyúti rendszer hibái. Méhen belüli fertőzés - bárányhimlő.
Hagyományosan az orosz irodalomban a kifejezés alatt "méhen belüli fertőzések"(IUI) olyan betegségekre utal, amelyekben a fertőzés a születés előtti időszakban vagy a szülés során következik be, és a fertőzés forrása az anya. Meg kell jegyezni, hogy az anyától származó gyermek méhen belüli fertőzése sokkal gyakrabban fordul elő, mint a fejlődés. Klinikai tünetek betegségek. Az intrauterin fertőzés tényének jelzésére gyakorlati orvoslás használja a kifejezést "méhen belüli fertőzés". Term "méhen belüli fertőzés"általában hivatkozni szoktak klinikai megnyilvánulásai a magzat és az újszülött fertőző betegsége, amelyet prenatálisan vagy röviddel a születés után észlelnek.
Méhen belüli fertőzés - rubeola
A tüdő röntgenfelvételein mikrobák és hálós árnyékok, sűrű pulzus, homályos szívverések láthatók. Paraklinikai vizsgálatok: hemogram - leukocytosis lázzal, limfomonocitózis, thrombocytopenia; kritikusan alacsony összfehérje és albumin. Diagnosztizálva újszülöttkori szepszis több szervben, légzési distressz szindróma, súlyos meningoencephalitis, agyvérzés. A negyedik születésnapon a gyermek végzetesen véget ér. A szülés során a gyermek alkalmazkodási nehézségeket tapasztal.
Az intrauterin fertőzés gyakorisága.Általános irodalmi adatok szerint az újszülöttek legalább 10%-a in utero fertőzött különféle vírusokkal és mikroorganizmusokkal. Az intrauterin fertőzés kockázata a kórokozó típusától, a terhes nő és a magzat kezdeti egészségi állapotától, valamint az adott földrajzi régió járványügyi helyzetétől függ. Terhes nők elsődleges fertőzése esetén nagyobb gyakorisággal figyelhető meg, mint látens vagy másodlagos vírusfertőzésben.
Intenzívvel intenzív osztály progresszív állapotromlást, fokozott sárgaságot, lázat és a szem lázas váladékát rögzítik. Az újszülöttet 30 órával intubálják, és megkezdődik a lélegeztetés. Ugyanakkor petechiális kiütés, generalizált ödéma, klónikus rángatózás jelentkezett Alsó végtagok, vérzik légutak. A születés utáni negyedik napon az LM-t izoláltuk vérkultúrákból, folyadékokból, szemekből, fülekből és légcsőből. A gyerek konzultál fertőző személy, az etiológiai kezelés megváltozik, a felületaktív anyagot kétszer adják be, de a tüdőfunkció változatlan marad.
Az intrauterin fertőzések jelentős ok reproduktív veszteségek. Így a korai újszülött morbiditás és mortalitás gyakorisága IUI-ban 5,3-27,4%, a halvaszületési arány pedig eléri a 16,8%-ot. A perinatális mortalitás szerkezetében a fertőzés 10,1%-ot tesz ki. Még jelentősebb szerepe a fertőző gyulladásos betegségek játszanak a perinatális morbiditás szerkezetében, ahol 20-38%-ot tesznek ki.
Az intrauterin fertőzés kezelése és monitorozása
A megfelelő antibakteriális és immunmoduláló terápia ellenére a gyermek a születést követő 12. napig függ a szobaszellőztetéstől. A felépülési periódus lassú, a gyermek izomtónusa csökkent, szívóreflex, tachydyspnoe, bőséges felső légúti szekréció és állandó pulmonális észlelés tapasztalható egy kis nedves sípoló krizmában. A 30. napon rokonok kérésére megírták, majd külön házban helyezték el egészségügyi ellátás. Kezelés: Alkalmazott szellőztetés; felületaktív anyag - kétszer; antibiotikumok - cefuroxim, amikacin, meropenem, fortum, ampicillin, linezolid, intravénás infúziókés vitaminok, flukonazol, humán albumin, 3 havi immunovenin, plazma transzfúzió és vérátömlesztés.
Ugyanakkor a fertőző faktor okozta perinatális patológia valós gyakorisága tisztázatlan, ami a szűrővizsgálatok hiányából, a fertőzés gyakorisága és a direkt morbiditás közötti eltérésből, valamint a gyakori látens lefolyásból adódik. kóros folyamat, objektív komplexitása antenatalis laboratóriumi diagnosztika. Ennek eredményeként
A gyermek szociális otthonban nevelkedik; A neuropszichés fejlődés eltérései súlyosak, a hydrocephalus továbbra is fennáll és mélyül. A listeriosis egy akut fertőző betegség, amelyben vérmérgezés alakul ki. klinikai kép több szerv károsodásával, időseknél a központi idegrendszer kiemelt érintettségével, terhes nők esetében pedig átültetett súlyos kár magzat, ami abortuszhoz vagy szélütéshez vezet.
Az etiológiai ágens korai azonosítása és megfelelő antibiotikum terápia renderelt kedvező befolyást listeriális fertőzésre. A szeptikus állapot és a paraklinikus paraméterek eltérései gyorsan megszűnnek, de a magzatra gyakorolt káros hatások megkövetelik a terhesség megszakítását orvosi indikációk. Az újszülötteknél leírt rendellenességek megfelelnek az irodalmi adatoknak. Ez felhívja az orvosok figyelmét, hogy a terhes nők úgynevezett "influenza szindróma" fennállása esetén is listeriózisnak kell tekinteni.
Így a fertőzések jelentős része ismeretlen marad, és a statisztikai elemzésben figyelembe veszik a születési aktus szövődményei, az intrauterin asphyxia, a légzési distressz szindróma és más kóros állapotok következményeként.
95,8%-ban a fertőzéses folyamat okozta halálozás oka a perinatális időszakban jelentkező állapot. Ezek közül a leggyakrabban feljegyzett: veleszületett tüdőgyulladás 47,5%, perinatális időszakra jellemző fertőzések 41,6%, újszülöttkori szepszis 6,7%.
A magzati fertőzés megelőzése
Az etiológiai finomítás és a megfelelő antibiotikum-terápia megóvja a magzatot a súlyos poligonális sérülésektől. Alapelvek és gyakorlat fertőző betegségek. Fertőző betegségek és terhesség. Az anya és a méhen belüli magzat fertőző betegségei. A listeriosisos megbetegedések száma Franciaországban és más európai országokban. Ásványolajjal kapcsolatos újszülöttkori listeriózis kitörése.
Listeria monocitogén fertőzés terhesség alatt - kortárs szempontok. Listeriosis terhesség alatt: esettanulmány. Klinikai megjelenés és kimenetel listeriosis esetén. Emiatt az anyáról gyermekre való terjedés megelőzése az egyik fontos összetevői perinatális ellátás. Ezért a perinatális gondozás egyik legfontosabb célja a fertőzés anyáról újszülöttre történő átvitelének megakadályozása.
Etiológia. A feltétel nélküli kórokozók listája meglehetősen kiterjedt, és több tucat fajt tartalmaz szinte minden organizmusosztályból, a vírusoktól a protozoákig és a gombákig.
A tünetekkel született gyermekek százalékos aránya bakteriális a méhen belüli fertőzések aránya 20-36%. Jelenleg számos aerob és anaerob bakteriális ágens szerepe bizonyított, elsősorban az opportunista mikroflóra képviselői: staphylococcusok, streptococcusok, coli, Klebsiella, Proteus, Enterobacteria, valamint nem spóraképző anaerob mikroorganizmusok. Meg kell jegyezni, hogy ebben a betegcsoportban a hüvelyi mikrobiocenózis összetételében általában jelentős zavarokat észlelnek (60-65%-ban vulvovaginális candidiasis vagy bakteriális vaginosis).
A szepszis lényege a szervezet gyulladásos reakciója egy fertőző ingerre, amely a baktériumok vérben való megjelenésével kapcsolatos. Legtöbbjüket a csecsemő fenyegeti, ami szervi elégtelenséghez vezethet. Az egyik legfontosabb klinikai kutatás kórtörténet, amelyben értékelni kell a terhesség és a szülés lefolyását. A korai újszülöttkori szepszis leggyakrabban az életnapok között fordul elő, de kivétel még a születés után néhány órával is. A késői újszülöttkori szepszis az élet napjai között jelentkezik.
Az újszülöttkori szepszis szövődményei
Az újszülöttkori szepszis egyéb szövődményei közé tartozik a légúti, szív- és érrendszeri, anyagcsere-szövődmények, osteomyelitis és mások.
Megelőző és megelőző intézkedések a fertőzés megelőzésére
Újszülött kezelése szepszis alatt. A szeptikus fertőzésben szenvedő újszülött egy közvetítő egységbe kerül, ahol egészségügyi személyzet figyeli és kezeli. Különösen fontos a gondos manipuláció, amely megkönnyíti a fájdalom észlelését ebben a betegségben. Amint az újszülött egészségi állapota javul, visszatér az anya szobájába.A bakteriális IUI klasszikus példája a listeriosis, amelyet a Listeria monocytogenes- rövid Gram-pozitív rudak (coccobacilli). A méhen belüli fertőzés egyéb bakteriális kórokozói közül az elmúlt években megnőtt a B csoportba tartozó streptococcusok szerepe, amelyek magzati patológiájában, különösen újszülötteknél, jelentős mértékben megnőtt az aminoglikozid antibiotikumok széles körű gyakorlati bevezetésének hátterében, amelyekben ezek a mikroorganizmusok természetesen ellenállóak. Jelenleg szoros összefüggést állapítottak meg a B csoportba tartozó streptococcusok újszülöttek által okozott fertőzéseinek gyakorisága és e baktériumok anyák genitális traktusában való hordozásának gyakorisága között. A B csoportú streptococcusok hordozásának kimutatásának gyakorisága terhes nőknél széles skálán mozog - 1,5-30%. A legveszélyesebb a masszív fókusz (több mint 10 5 CFU / ml) az anya nyaki csatornájában. Ilyen esetekben az újszülöttek több mint 60%-a fertőzötten születik. Az e baktériumok által okozott fertőzések klinikai megnyilvánulásai újszülötteknél változatosak - a helyi bőrtől kezdve
A nők a terhesség alatt a kórokozók széles körének vannak kitéve. A fertőzés kialakulása ugyanolyan gyakori, mint a terhesség. A kivétel az megnövekedett kockázat magzati fertőzés. Egyes kórokozók fokozott affinitást mutatnak a placenta trofoblasztjaihoz, ami gyulladást, majd magzati fertőzést okoz. A fertőzés előfordulhat prenatálisan, perinatálisan vagy újszülöttkori időszakban. A fertőző ágens anyáról magzatra történő átvitelét vertikálisnak nevezzük.
A prenatális fertőzéseket embriopátiákra és fetopátiákra osztják, attól függően, hogy a terhesség mely időszakában jelentkezik a rendellenesség. Az embriopátiák a terhesség első trimeszterében fordulnak elő, és teratogén fejlődési rendellenességek jellemzik. A blasztogenezis során az ágens bejut az embrióba, és általában meghal. Az organogenezis stádiumában az anyai ágens hematogén úton kerül a magzatba, azonban a méhlepény, beleértve a magzati placentális keringést is, még nem fejlődött ki teljesen, ami korlátozza a kórokozó átjutását a magzatba.
súlyos fulmináns szeptikus folyamatokhoz és agyhártyagyulladáshoz, amelyet a koraszülöttek magas mortalitása (akár 80%) kísér.
Az elmúlt években a perinatális patológia felépítésében a jelentősége a ssualno-transzmissziós intracelluláris fertőző ágensek: mikoplazmák, ureaplazmák és chlamydia. A nemi urea- és mycoplasmosis okozta méhen belüli fertőzés gyakorisága terhes nőknél 40-50%, chlamydia esetén pedig eléri a 70,8%-ot.
A fetopathia a terhesség hónapjától jelentkezik, és nincs anatómiai rendellenesség, az érintett szervek működése általában károsodik. A fertőzés hematogén úton, röviddel a születés előtt és után történik. Egy intracelluláris patogén ágens bejut a magzati placenta keringésébe. A magzati teratogenezisnek többtényezős okai vannak, beleértve a genetikát, a gyógyszereket és a környezeti expozíciót.
A terhesség alatti fertőzés következménye lehet. Méhen belüli növekedési retardáció vagy koraszülés miatt alacsony születési súlyú újszülött születése. Teratogén malformáció – a legjobban dokumentált teratogén a rubeolavírus. Aktív veleszületett fertőzések - születés előtt jelentkeznek, és a fertőző ágens még születés után is jelen van. Abortusz, koraszülés vagy újszülött halála. . Prenatális fertőzés A krónikus veleszületett szindróma legalább egy hónapos fertőzést jelent, amelynek tünetei a születéskor nyilvánvalóak voltak.
A perinatális fertőzések jelentős részét különféle vírusok, amelyek közül a legfontosabbak a citomegalovírusok, a herpes simplex, a rubeola, az enterovírusok (ECHO, Coxsackie), a hepatitis B, a humán immundeficiencia vírus. Ezenkívül az influenza, a kanyaró, a poliomyelitis, a papilloma és a parvovírusok befolyásolják az újszülöttek szaporodási veszteségének és megbetegedésének növekedését.
A krónikus veleszületett szindróma aktív fertőzésként jelentkezhet aktív gyulladásos válasz jeleivel vagy a gyógyulás jeleivel. Egyéb krónikus veleszületett fertőzések tüneteket jelezhetnek veleszületett rendellenességek vagy fertőzés következtében jelentkező szervi érintettség jelei.
Perinatális streptococcus fertőzések. A fertőzés a múltban csak a műtéti beavatkozásokés a szülés. A perinatális fertőzések fő etiológiai ágense a streptococcusok voltak. Ezek a tények aggodalomra adnak okot az újszülöttek súlyos szülés utáni fertőzésének kockázatával kapcsolatban.
Az elmúlt években megnőtt a helyi formájú herpetikus elváltozásban szenvedő betegek száma, ami meghatározza az újszülöttek herpeszfertőzésének gyakoriságának növekedését. A nemi szervek vírusának vereségét a terhes nők 7% -ánál észlelik. A herpesz a klasszikus krónikus fertőzés egyik példája, amelyben a kórokozó egész életen át jelen van a gazdaszervezetben. Körülbelül 70 vírustípust izoláltak ebből a csoportból, amelyek közül 4 érinti az embereket: a herpes simplex vírus I és II szerotípusa, a varicella-zoster vírus, az Epstein-Barr vírus és a citomegalovírus (mindhárom izolált törzs - Devis, Kerr és AD189) klinikai jelentősége.
Ezeket az ajánlásokat egy munkacsoport dolgozta ki, és a Lengyel Nőgyógyász Társaság és a Lengyel Újszülöttek Társasága hagyta jóvá. A kórházi fertőzések korábban csak sebészeti beavatkozásokkal és vajúdással voltak. Fő etiológiai tényezők ez a fertőzés streptococcus volt.
Toxoplazmózis: a fertőzés jellemzői
Ez nagy aggodalomra ad okot az újszülöttek súlyos perinatális fertőzéseinek kockázatával kapcsolatban. Az ilyen irányelveket egy munkacsoport készítette, és a Lengyel Nőgyógyász Társaság és a Lengyel Újszülöttek Társasága hagyta jóvá. Az újszülöttkori időszak az az időszak, amikor a gyermek teste az intrauterinból a konfliktusmentes életbe való átmenet után alkalmazkodik az új körülményekhez. A statisztikák szerint az élet első 28 napját fedi le.
A lakosság körében meglehetősen gyakoriak enterovírus fertőzések. Az intrauterin fertőzések kórokozójaként az echovírusok és a Coxsackie vírusok a legnagyobb érdeklődésre számot tartóak. A kísérlet igazolta az A 13, A 3, A 6, A 7, B 4 és B 3 típusú Coxsackie vírusok, valamint a 9. és 11. típusú echovírusok etiológiai jelentőségét.
Külön figyelmet érdemelnek az AIDS-et okozó retrovírusok. A HIV-fertőzött anyák gyermekeinek akár 50%-a megfertőződik a születés előtti, szülésen belüli vagy korai újszülöttkori időszakban. A szeropozitív anyáktól származó újszülöttek betegségeinek előfordulása széles skálán mozog - 7,9 és 40% között.
Az újszülöttek fertőzésekre való érzékenysége az éretlenség eredménye immunrendszer, különösen azoknál, akiknél gyakran alkalmaznak invazív diagnosztikai és terápiás eljárásokat. A fertőzés kifejezés a következőkre oszlik. Nagyon korai fertőzések. korai fertőzések.
A fertőzések kezelésének alapelvei
fertőzések késői kezdés. Anyai oldalon - véráramlás, adenoma, összeomlás, perinatális fertőzés. A perinatális fertőzések olyan fertőzések, amelyek a szülés során az újszülött nyálkahártyájának az anya nemi traktusában jelenlévő mikroorganizmusokkal való érintkezése következtében alakulnak ki, így a perinatális fertőzés fő oka az anya méhének flórája, ritkán a környezet, különösen a kórház.
A legmagasabb érték között gombás Az IUI kórokozói a nemzetség gombáinak széles körben elterjedt képviselőivel rendelkeznek Candida. Cryptococcosis, coccyoidosis, aspergillosis és hisztoplazmózis terhes nőknél
nyh gyakran előfordul az immunhiány hátterében. Fel kell hívni a figyelmet arra a tényre, hogy a terhesség alatt a hüvelyi candidiasis klinikai megnyilvánulásainak gyakorisága meredeken növekszik. III trimeszter eléri a 31-33%-ot. Ez a jelenség a hüvelyi epitélium sejtjei által a glikogén felszívódásának megsértésével, valamint a mucin képződésének növekedésével jár, ami a „hígító” hatás miatt előre meghatározza az aktív hatóanyagok koncentrációjának csökkenését. a helyi immunitás tényezői a hüvelyi közegben - lizozim, kationos fehérjék, antitestek, stb. tápanyagok glikogén formájában, a helyi immunitás gyengülésével kombinálva, kedvező feltételeket teremtenek a gombaflóra patogén hatásának megvalósításához. A DNS-diagnosztika szerint a hüvelyi szülés során a candidiasisban szenvedő betegek anyjától származó újszülöttek kontaminációja megközelíti a 100%-ot, az újszülöttkori időszak végére pedig már csak 35%-ban figyelhető meg a gombák spontán eliminációja, ami a candidiasis kialakulására utal. a maradék. A klinikailag kifejezett candidiasis gyakorisága újszülötteknél az első 35 napban megközelíti a 20-30% -ot, és a kezelés ellenére 1 hónap elteltével minden ötödik megfigyelésben megfigyelhető. gombás fertőzés nemcsak a szájüregi, nemi és bőr megnyilvánulásai candidiasis újszülötteknél, de a magzat méhen belüli fertőzéséhez is vezethet, szisztémás mycosis kialakulásával, mély tüdő-, agykárosodással, valamint spontán vetéléshez (gyakrabban a II trimeszterben, 14-25 héten belül).
Citomegalovírus fertőzés újszülötteknél
Fájdalom és belső környezete, amíg a ciszták fel nem törnek. Másrészt az anya útjában sok olyan mikroorganizmus található, amely fertőzést okozhat az újszülöttben. Általában egészséges felnőttek felszínén helyezkednek el, de bizonyos körülmények között képesek behatolni a gazdaszövetekbe, elkerülni az immunválaszokat és megfertőzni. Fő klinikai formák ezen fertőzések közül a nekrotizáló fasciitis és a toxikus sokk szindróma. Kommenzálisként ez a baktérium az alsót is elfoglalhatja gyomor-bél traktus, végbélnyílás, női hüvely.
Végül perinatális fertőzések keletkeznek protozoák, treponemák és rickettsiák. Ebben a csoportban a legfontosabb toxoplazmózis, az intrauterin fertőzés gyakorisága, amelyben körülbelül 40%. Ezenkívül az elmúlt években a szifilisz gyakoriságának növekedése irányába mutatott tendencia. A veleszületett szifilisz az újszülöttek több mint 50%-ánál fordul elő olyan beteg anyáktól, akik nem részesültek megfelelő kezelésben.
Ezt elősegíti a szexuális arányok magas gyakorisága. A fő kórokozók a poliszacharidok, egyéb hemolizinek és a neuraminidázok. A policisztás antigének elleni antitestek jelenléte az anya szérumában megvédi a gyermeket a fertőzéstől. A fertőzésre adott válasz antigén-specifikus. Csecsemőknél a fertőzés leggyakrabban a szülés során következik be, ritkán korai cisztás fibrózis következtében.
Az embrió csontjainak gyulladása. Korai köhögés. A fertőzés lehet tünetmentes hordozó, korai fertőzés - leggyakrabban újszülöttek szepszisben nyilvánulnak meg - agyhártyagyulladás és fertőző betegség. A korai fertőzés, amely gyorsan növekvő légzési elégtelenségben, rossz neurológiai állapotban, táplálkozási rendellenességekben és mortalitásban nyilvánul meg, 5 és 20% között mozog. Az ilyen fertőzések okozta halálozás 2-6%.
Fontos megjegyezni, hogy a legtöbb esetben a méhen belüli fertőzés több kórokozó társulásának köszönhető, vagy vegyes (vírus-bakteriális, bakteriális-gombás). Az intrauterin fertőzés miatti születés előtti mortalitás szerkezetében 27,2% esik rá vírusos fertőzés, 26,3% - kevert és 17,5% - bakteriális.
1971-ben azonosították a fertőzések egy csoportját, amelyek a kórokozók szerkezetében és biológiai tulajdonságaiban mutatkozó jelentős különbségek ellenére hasonló klinikai megnyilvánulásokkal rendelkeznek, és tartós szerkezeti hibákat okoznak a különböző magzatok magzatában. szervrendszerek, melyek közül a legfontosabbak a központi idegrendszer elváltozásai. Ennek megjelölésére fertőző csoport A.J. Nahmias (1971) javasolt egy rövidítést FÁKLYA. Ez a komplex a következő intrauterin fertőzéseket egyesíti: T- toxoplazmózis, R- rubeola (rubeola), C- citomegalovírus fertőzés, H- herpeszvírus fertőzés.
Az elmúlt 15 évben a perinatális fertőzések etiológiai szerkezete megváltozott. Ez részben a megnövekedett lehetőségeknek köszönhető specifikus diagnózis, elsősorban mycoplasmosis, chlamydia, citomegalia, herpetikus és streptococcus B fertőzés A kórokozók, különösen a Listeria (Ailama-
Zyan E.K., 1995).
Ellenére széleskörű kórokozók, meg kell jegyezni, hogy minden méhen belüli fertőzésnek közös jellemzői vannak:
Látens vagy törölt lefolyás, ami jelentősen megnehezíti a diagnózist (különösen a kórokozó intracelluláris lokalizációja esetén - chlamydia, mikoplazmák, vírusok stb.), és nem teszi lehetővé az etiotrop terápia időben történő megkezdését;
A látensen perzisztens fertőzés aktiválása lehetséges a homeosztázis bármely megsértésével terhes nőknél (vérszegénység, hipovitaminózis, túlterheltség, stresszes helyzetek, nem fertőző természetű extragenitális betegség dekompenzációja).
A méhen belüli fertőzés útjai és a magzat fertőzésének mechanizmusa
Az intrauterin fertőzés a következő módokon fordul elő: "emelkedő- az alsó specifikus elváltozás jelenlétében
a nemi traktus szakaszai (34. ábra); "hematogén(transzplacentáris) - a legtöbb esetben egyes mikroorganizmusok azon képessége miatt, hogy hosszú ideig fennmaradnak a perifériás vér limfocitáiban;
transzdeciduális(transzmurális) - fertőzés jelenlétében az endometriumban;
Rizs. 34. A felszálló intrauterin fertőzés patogenezise
ereszkedő- a gyulladásos fókusz lokalizációjával a méh függelékeinek területén;
*fertőző- az újszülött közvetlen szennyeződése a szülőcsatornán való áthaladáskor;
vegyes.
Az opportunista kórokozókkal járó bakteriális méhen belüli fertőzés elsősorban a miatt alakul ki felszálló fertőzés a szülőcsatornából. Ez az út a mikoplazmákra, chlamydiákra és a nemzetség gombáira is jellemző Candidaés csak bizonyos vírusok, különösen a herpes simplex. Hajlamosító tényezők az urogenitális fertőzések, isthmic-cervicalis elégtelenség, részleges hártyarepedés, idő előtti vízkibocsátás, chorion biopszia, magzatvíz vizsgálat.
A felszálló fertőzés akkor fordul elő leggyorsabban, ha a membránok megsérülnek. Egy nő magzatvize késői időpontok a terhességnek van antimikrobiális hatása, amely azonban gyengén kifejeződik, és csak késleltetheti (de
ne gátolják) a mikroorganizmusok szaporodását. A bakteriosztatikus hatás nagyon rövid ideig tart (3-12 óra). Gyulladásos változások a méhnyakcsatornával szomszédos membránok területén mindig korábban találhatók, mint a méhlepény boholyaiban. A legtöbb opportunista mikroorganizmus alacsony virulenciája miatt a magzati membránok kívülről érintetlenek maradnak. Ugyanakkor a membránok számos opportunista mikroorganizmus számára átjárhatóak, így a magzat fertőzése akár egész magzati hólyaggal is előfordulhat. A kórokozó behatol a magzatvízbe, intenzív szaporodása és felhalmozódása következik be. A fertőzés fókusza kialakul, és a magzat fertőzött környezetben van. Az úgynevezett fertőzés szindróma magzatvíz.
A magzat fertőzése a fertőzött vizek lenyelésével és felszívásával történik, ami az újszülöttben való megjelenéshez vezet. méhen belüli fertőzés jelei(tüdőgyulladás, enterocolitis, vesiculosis, omphalitis, conjunctivitis stb.). Ugyanakkor a mikroorganizmusok a membránokon keresztül vagy azok között terjedve elérik a placenta alaplemezét. (deciduitis). A korionlemez és a köldökzsinór elemei a fertőzött magzatvízzel való érintkezéskor megfertőződnek. A gyulladásos reakció további terjedése chorionitis kialakulásához vezet (placentitis), amely az intervillous tér leukocita infiltrációjában és a chorionlemezben endovasculitisben nyilvánul meg. Vasculitis a deciduában, a szárban és a végbolyhokban érelzáródáshoz, szívinfarktus megjelenéséhez, meszesedéshez, masszív fibrinoid lerakódásokhoz vezetnek, amelyek megnyilvánulhatnak « idő előtti érés placenta."
A "magzatvíz fertőzés" szindróma megnyilvánulásai a chorionamnionitis mellett a következőket tartalmazzák polihidramnion, amely a betegek 5,5-63,6%-ánál már a terhesség első trimeszterének végén kimutatható. Kialakulásának oka az amnionitis hátterében a magzatvíz termelésének és felszívódásának arányának megváltozása a magzatvíz epitélium sejtjei által. oligohidramnion méhen belüli fertőzés esetén általában másodlagos, és a vesekárosodás megnyilvánulása (csökkent diurézis placenta elégtelenséggel), ill. húgyúti magzat (obstruktív hydronephrosis).
Képződés placenta elégtelenség. Az IUI-ban előforduló placenta elégtelenség tünetegyüttesének genezisében a főszerep az érrendszeri betegségeké (vaszkulitisz és a méhlepény magzati részének ereinek trombózisa a chorionitis (placentitis) hátterében). A sejt morfofunkcionális állapotának változásai A méhlepény-gyulladás hátterében a lipidperoxidációs folyamatok aktiválódása miatti membránok is fontosak A placenta elégtelenség fő megnyilvánulásai krónikus magzati hipoxia és intrauterin növekedési retardáció, amely a fertőzés időpontjától függően szimmetrikus (fertőzés a placentáció befejezése előtt) vagy aszimmetrikus.
Az intrauterin fertőzés tipikus megnyilvánulása az vetélés terhesség. A megfigyelések 70%-ában a terhesség spontán megszakadása a későbbi szakaszokban és a koraszülés azzal kezdődik. a magzatok idő előtti megrepedése
kagylókés csak 30% -ban - a méh összehúzódási aktivitásának növekedésével. Korai fejlődés munkaügyi tevékenység a membránok idő előtti megrepedése pedig a prosztaglandin kaszkádot beindító bakteriális foszfolipázok hatásának és a gyulladásos toxinok membránokat károsító hatásának köszönhető.
Tekintettel arra, hogy a gram-negatív baktériumok foszfolipázai hozzájárulnak a felületaktív anyag pusztulásához a magzat tüdejében, az újszülött fejlődik. légzési rendellenességek.Így a felszálló fertőzés következő fejlődési sorrendje épül fel: colpitis, cervicitis - magzatvíz fertőzés - magzatvíz hám károsodása - hártyagyulladás - chorionlemez amnionitis - köldökzsinór perivasculitis - légúti károsodás , tüdő, emésztőrendszerés bőr - születés előtti magzati halál.
Csoportos nők mikrobiológiai vizsgálata során megnövekedett kockázat IUI fejlesztés bakteriális etiológia megállapították a nők urogenitális traktusának mikroflórájának és a gyermekeiktől izolált mikroorganizmusok fajösszetételének azonosságát. Az IUI klinikai megnyilvánulásaival rendelkező újszülötteknél a masszív vetés főleg a belső üregekben figyelhető meg (gyomortartalom, nasopharyngealis tamponok). Leggyakrabban a placenta anyai felületéről és a köldökzsinórvérről származó kenettenyészetek maradnak meg
sterilek, a magzatvíz és a méhlepény termőfelülete rendelkezik legmagasabb pontszám mikrobiális kolonizáció. Ez bizonyítja a magzat fertőzésének túlnyomóan felszálló útját és a magzatvíz vezető szerepét a magzat fertőzésében.
Mert hematogén a magzat fertőzése leginkább az anya testében lévő, extragenitálisan elhelyezkedő fókusz jelenlétére jellemző. A kórokozó, áttörve a placenta gátat, behatol a magzat véráramába. Hematogén fertőzés esetén gyakran előfordul a magzati test általános elváltozása - intrauterin szepszis. Minden valódi veleszületett vírusfertőzés, a mycoplasmosis, a chlamydia, valamint az olyan specifikus méhen belüli fertőzések, mint a listeriosis, a szifilisz és a toxoplazmózis, transzplacentális fertőzési úttal rendelkeznek.
A hematogén útvonalat a placenta méhágy vasculitisének túlsúlya jellemzi, majd - intervillusitis kialakulása, a chorion lemez vasculitise, majd - a köldökzsinór phlebitis és endarteritis, a máj, az agy fertőzése, más szervek károsodása a magzaté - születés előtti halál.
A megvalósításhoz transzdeciduális (transzmurális) a fertőzés útja megköveteli a fertőzés fókuszának jelenlétét az endometrium alatt. A magzat hasonló fertőzési útja leggyakrabban olyan betegeknél fordul elő, akiknek genitális-gyulladásos betegségei voltak.
VAL VEL ereszkedő méhen belüli fertőzéssel, melyben a kórokozó behatolása a magzati petesejtbe ezen keresztül történik a petevezetékek, a klinikai gyakorlatban a szervek akut sebészeti patológiájában szenvedő betegekkel kell foglalkozni hasi üreg gonorrheás, mycoplasmalis vagy chlamydia etiológiájú akut vagy krónikus salpingo-oophoritis. A klasszikus példa az akut vakbélgyulladás, míg a magzat károsodásának mechanizmusa a felszálló fertőzéséhez hasonlít.
A MAGZAT IMMUNRENDSZERE
Az érett immunválasz több sejttípus közötti kölcsönhatások összetett sorozatát foglalja magában. Az immunválaszban részt vevő egyes sejtek érésének folyamata a magzati élet korai szakaszában kezdődik. Az emberi immunrendszer progenitor sejtjei a magzat csontvelőjében és májában termelődnek. A T- és B-limfocitákra jellemző hisztokompatibilitási markerek és antigének már a terhesség 8-10 hetében kimutathatók a limfocitákon. Ahogy az immunrendszer sejtjei a makrofágokon, valamint a T- és B-limfocitákon érnek, egyre több receptor és hisztokompatibilitási marker jelenik meg, azonban a teljes érés csak körülbelül 2 évvel a születés után fejeződik be.
Tipikus esetekben már a terhesség második felében megfigyelhető a placentán áthaladó fertőző ágensekre adott válasz. Ez a fajta immunválasz általában az IgM osztályba tartozó antitestek képződésében nyilvánul meg, de kialakulhatnak IgG osztályú antitestek is. A magzati immunválasz IgG antitestek formájában történő azonosítása nehezebb a passzív anyai IgG antitestek jelenléte miatt.
Az anyai IgG antitestek a terhesség közepe táján kezdenek átjutni a placentán. A szülés során a gyermek vérében az IgG (főleg az anyai immunglobulinok) koncentrációja megegyezik az anya vérének megfelelő koncentrációjával, sőt meghaladja azt. Ez azt jelenti, hogy a gyermekben az anya szervezetében képződött összes IgG antitest megvan. Az anyai IgA és IgM antitestek nem jutnak át a méhlepényen, és ha ezekhez az osztályokhoz tartozó antitesteket találnak egy gyermekben, ez azt jelenti, hogy azok a gyermek testében keletkeztek.
Az IgA antitestek képződése gyakran még nem alakul ki teljesen a szülés idejére. Kimutatták, hogy ennek a rendszernek a teljes fejlődése az élet első hét évében folytatódhat. A magzat immunitásának fő forrása tehát az anyai IgG antitestek méhlepényen keresztül történő átvitele, bár már a fejlődés elég korai szakaszában immunrendszere képes saját védelmet kialakítani.
Az anya és a magzati magzat humorális és sejtes immunitása vizsgálati eredményeinek tanulmányozásában és értelmezésében jelentkező nehézségek új megoldásokat kerestek az immunreaktivitás felmérésére.
a terhesség alatti fertőző folyamat hátterében. Így számos pro- és gyulladásgátló citokint (interferonok, interleukinek, tumornekrózis faktor) értékeltünk a magzat, az anya és az újszülött különböző terhességi periódusaiban. Mivel a citokinek és az interferonok minden immunreakció univerzális szabályozói, mind a sejtes, mind a humorális, vizsgálatuk lehetővé teszi a legfontosabb klinikai probléma megoldását - van-e fertőzés a magzatban, és szükséges-e kezelést előírni? Bebizonyosodott, hogy az interleukin-4 szintjének csökkenése a gamma-interferon és a tumor nekrózis faktor koncentrációjának növekedésével kombinálva az anya vérében 86,4% méhen belüli fertőzés jelenlétét jelzi. Az ilyen vizsgálatok lehetővé teszik az újszülött fertőzési kockázatának non-invazív értékelését.
Patogenezis. A magzat intrauterin fertőzésének patogenezisében jelentős szerepet kap a kórokozó és a magzat közvetlen kölcsönhatása. A méhen belüli fertőzés során észlelt károsodások köre nagyon széles, és a morfogenezis jellemzőitől és a magzati reakciók jellemzőitől függ a méhen belüli fejlődés egy adott időszakában, a károsító tényező sajátosságaitól és időtartamától.
A kórokozó virulenciája és a magzati károsodás súlyossága közötti kapcsolat nem mindig egyenes arányos. Gyakran törölt szivárgó ill enyhe fertőzés az anyában toxoplazma, listeria, mikoplazma, chlamydia, a nemzetséghez tartozó vírusok vagy gombák által okozott Candida magzati halálhoz vagy születéshez vezethet súlyosan beteg gyermek. Ennek oka az egyes embrionális szövetek kórokozóinak tropizmusa, valamint az a tény, hogy a magas metabolikus aktivitású magzati sejtek kedvező környezetet jelentenek a mikrobák szaporodásához.
A bakteriális fertőző ágens károsító hatása egy destruktív kifejlesztésén keresztül valósulhat meg gyulladásos folyamat különböző szervekben strukturális vagy funkcionális hiba kialakulásával és közvetlen teratogén hatás révén perzisztens szerkezeti változások fejlődési rendellenességek formájában. A vírusos ágensek általában halálos rendellenességeket vagy fejlődési rendellenességeket okoznak a mitotikus sejtosztódás elnyomásával vagy közvetlen citotoxikus hatásokkal. A gyulladás után kialakuló folyamatok javítása
Eszem, gyakran szklerózishoz és szövetek meszesedéséhez vezet, ami szintén megzavarja a hisztogenezis folyamatát.
Az embriogenezis időszaka a terhesség első 3 hónapját öleli fel, a károsító tényezők hatására a legérzékenyebb szakasz az organogenezis első 3-6 hete (a fejlődés kritikus időszaka). A beültetés során a károsító tényezők hatására jelentősen megnő az érzékenység. Az ekkor fellépő fertőző embriopátiákra jellemző a deformitások előfordulása (teratogén hatás), ritkábban figyelhető meg az embriotoxikus hatás. Mindenekelőtt azokat a szöveteket érintik, amelyek az ágens hatásának időpontjában aktív differenciálódási folyamatban voltak. Nál nél különféle testek A könyvjelző periódusai időben nem esnek egybe, így a károsító szerrel való érintkezés időtartama a léziók sokaságától függ.
A korai magzati időszak kezdetével a magzat specifikus érzékenységet alakít ki az intrauterin fertőzések kórokozóival szemben. A 13 hét után fellépő magzati elváltozásokat "fetopátiának" nevezik. A szeptikus etiológiájú fetopátiával lehetséges a malformációk kialakulása. Ennek morfológiai alapja az alteratív és proliferatív folyamatok, amelyek a természetes csatornák és nyílások eltüntetéséhez vagy szűküléséhez vezetnek. Az ilyen változások a már kialakult szerv további fejlődésének megsértéséhez vezetnek. Tehát a húgyúti fertőzés hydronephrosishoz, átvitt meningoencephalitishez - hydrocephalushoz vezethet, a Sylvian vízvezeték szűkülése vagy eltüntetése hátterében.
Amikor a terhesség 27. hete után fertőződik, a magzat képes lesz specifikusan reagálni a fertőző ágens bejuttatására leukocita infiltrációval, humorális és szöveti változásokkal. A fertőző ágens károsító hatása ebben az esetben funkcionális hibák formájában jelentkezik.
Azt is meg kell jegyezni, hogy az IUI patogenezisében fontos kapcsolatok a fertőző ágens anyagcseretermékeivel való mérgezés, a hipertermia és a hipoxémia. A fenti tényezők méhen belüli magzatra gyakorolt hatása a tüdő, a vesék és az agy növekedésének és differenciálódásának késleltetésében nyilvánul meg, még a méhen belüli fertőzés egyéb megnyilvánulásainak hiányában is.
Klinikai tünetek méhen belüli fertőző betegség újszülöttben, vagy már születéskor jelen van, vagy manifesztálódik
lyatsya az élet első 3 napjában (leggyakrabban az 1-2. napon). A szülés utáni időszakban történő fertőzés esetén a fertőző folyamat tüneteit később észlelik. Hosszabb lappangási idő lehetséges méhen belüli fertőzések ("késői" agyhártyagyulladás, osteomyelitis, chlamydia elváltozások stb.), vagy éppen ellenkezőleg, nosocomiális fertőzés korai megnyilvánulása esetén (különösen koraszülötteknél).
Az újszülöttek bakteriális méhen belüli fertőzésének leggyakoribb klinikai megnyilvánulása az élet első napjaiban az ún. fertőzés szindróma. Egy ilyen gyereknek közös klinikai tünetek mérgezés jeleit tükrözi, és általános letargiában, csökkent izomtónusban és reflexekben (különösen a szopási reflexben), regurgitációban, a mell megtagadásában nyilvánul meg. Oldalról a szív-érrendszer- szívhangok süketsége, hipoxiás jellegű EKG-változások. Pallor megfigyelte bőr, a légzés ritmusának és gyakoriságának megsértése, cianózis rohamok. A fertőzés egy szeptikus folyamat kialakulását eredményezheti, melynek megvalósításában fontos az újszülött élete első óráiban kialakult állapota, a kórokozó dózisa. A koraszülöttség, a légzési és hemodinamikai zavarok, a koponyaűri sérülések, a hipoxia hozzájárul az újszülött testének ellenálló képességének csökkenéséhez, és kedvező hátteret jelent a fertőzés kifejeződésének, szeptikus folyamat jellegét kölcsönözve.
Az újszülötteknél az intrauterin fertőzések specifikus megnyilvánulásai eltérőek - az enyhe helyi formáktól a súlyos szeptikusakig.
A veleszületett bakteriális vagy gombás bőrelváltozások klinikai megnyilvánulásai újszülöttben lehetnek vesiculopustulosis. Százalék pozitív eredményeket a gyermek születése után közvetlenül vett hólyagok tartalmának mikrobiológiai vizsgálata alacsony, ezért vitatható, hogy az "aszeptikus" vezikulákat egy veleszületett fertőzésnek tulajdonítsuk, vagy a bakteriális allergia megnyilvánulásaként tekintsük kiütés megjelenésével a bőrön. A valódi (mikrobiológiailag igazolt) vesiculopustulosis prenatálisan fertőzött gyermekeknél, általában az 1. és a 2. életnap végén jelentkezik, és a kórokozók leggyakrabban streptococcusok.
ki B és D csoport, Escherichia, élesztőszerű gombák (Ankirskaya A.S. et al., 1989).
Kötőhártya-gyulladás, rhinitis és otitis,életének 1-3. napján jelent meg, méhen belüli fertőzés megnyilvánulása is lehet. Veleszületett kötőhártya-gyulladás esetén az opportunista mikroorganizmusok jelenlétére vonatkozó szemváladék mikrobiológiai vizsgálata mellett gonokokkusz-vizsgálat céljából kenet vétele szükséges.
Méhen belüli tüdőgyulladás- az újszülöttek veleszületett fertőzéseinek leggyakoribb formája. Gyermekeknél a születés pillanatától kezdve a légzési elégtelenség jelei figyelhetők meg: légszomj, cianózis, gyakran az ütőhangszerek tompasága és kis, bugyborékoló nedves hangok. Az élet első óráiban végzett röntgenvizsgálat megerősíti a tüdőgyulladás gócainak jelenlétét. A veleszületett aspirációs tüdőgyulladás az élet 2. vagy 3. napján is megjelenhet. A tracheobronchiális traktusból származó aspirátum mikrobiológiai vizsgálata során újszülötteknél aspirációs tüdőgyulladás Leggyakrabban gram-negatív baktériumokat izolálnak, míg kórházi újszülöttkori tüdőgyulladás esetén a Staphylococcus aureust. A veleszületett tüdőgyulladás lefolyása súlyos, mert az aspiráció következtében a tüdő nagy területei (alsó és középső lebeny) leállnak a légzéstől aspirációs tömeggel - fertőzött, meconium keveréket tartalmazó magzatvíz, magzati bőr - hörgőelzáródás miatt. Mérleg.
Enterocolitisújszülötteknél méhen belüli fertőzés jellege is lehet, amikor a kórokozó a magzatvízzel együtt behatol a gyomor-bél traktusba. A veleszületett enterocolitisre a következő klinikai megnyilvánulások jellemzőek: lassú szívás, regurgitáció, puffadás, a máj és a lép megnagyobbodása, az elülső vénás hálózat kitágulása hasfal, gyakori folyékony széklet. A dyspeptikus tünetek általában az élet 2-3. napján alakulnak ki. Fontos a béltartalom mikrobiológiai vizsgálata (a bél mikrocenózis kialakulásának megsértésének jelei - a Klebsiella, Proteus, Pseudomonas aeruginosa mennyiségi túlsúlya).
A központi veresége idegrendszerújszülötteknél az IUI-val elsődleges (meningitis, encephalitis) és másodlagos is lehet, mérgezés következtében. Behatolás izgat-
la a magzati agyban leggyakrabban a CSF pályák mentén fordul elő, így a fertőzés a fej membránjában, ill. gerincvelőés a formában folyik agyhártyagyulladásés meningoencephalitis. Az agy laterális kamráinak choroid plexusaiban is változások következnek be, amihez veleszületett hydrocephalus is társulhat.
Vérmérgezésújszülöttnél nehéz diagnosztizálni a szervezet alacsony reaktivitása miatt. A betegség kezdetén a klinikai megnyilvánulások enyhék lehetnek, csak az általános mérgezés jelei lehetnek, nyilvánvaló fertőzési góc nélkül (a "fertőzés" szindróma). Figyelni kell az olyan tünetekre, mint a letargia, rossz szopás, regurgitáció, késleltetett felépülés vagy másodlagos fogyás, a köldökseb késleltetett gyógyulása, omphalitis kialakulása. Az újszülöttek fertőző mérgezésének jellemző tünetei a légúti és szöveti anyagcsere zavarai. Van egy halvány cianotikus, szürkés árnyalatú, a bőr színe kifejezett érmintázattal (bőrmárványosodás). A mérgezést a máj kiválasztó funkciójának megsértése, elhúzódó sárgaság kialakulása kíséri. A szepszis tünetei közé tartozik a lép és a perifériás nyirokcsomók megnagyobbodása is. Tájékoztató jelek az ödéma bőr alatti szövet, hipokróm vérszegénység, vese- és májműködési zavar, víz-só és fehérje anyagcsere (hipoproteinémia) (Ankirskaya A.S. és
et al., 1989).
Azt is figyelembe kell venni nem specifikus megnyilvánulások méhen belüli fertőzés. Az ebbe a csoportba tartozó újszülötteknél az alkalmazkodási reakciók olyan létfontosságúak fontos rendszerek központi idegrendszeri, légzőszervi, szív- és érrendszeri, endokrin és immunrendszerként. Gyakran alacsony az Apgar-pontszám a születés utáni első percben. A korai újszülöttkori időszakban gyakran előfordulnak alkalmazkodási kudarcok hipoxiás szindróma, légzőszervi és szív- és érrendszeri rendellenességek szindróma, mellékvese és agyi patológia formájában. Szem előtt kell tartani az olyan megnyilvánulások lehetőségét, mint a veleszületett alultápláltság, ödémás szindróma, hiperbilirubinémia, DIC vérszindróma.
BELSŐ FERTŐZÉSEK ELŐSZÜLETÉSI DIAGNOSZTIKA
Tekintettel a patológia klinikai megnyilvánulásainak nem specifikusságára, a prenatális diagnózis a legnehezebb.
A legracionálisabb az intrauterin fertőzések szakaszos diagnózisa.
A első fázis az anamnesztikus adatok gyűjtése és az általános klinikai vizsgálat alapján meghatározzák az intrauterin fertőzések kialakulásának magas kockázati csoportját. Ebbe a csoportba tartoznak a betegek:
Extragenitális fertőzési gócok, különösen a fertőző folyamat terhesség alatti súlyosbodása esetén, valamint azok, akik terhesség alatt akut légúti vírusfertőzést tapasztaltak;
VAL VEL korai kezdés szexuális élet és szexuális partnerek gyakori cseréje, akiknél urogenitális fertőzések epizódjai voltak;
Azok, akiknek gyulladásos megbetegedései voltak a méhben és függelékeiben, colpitisben, szexuális úton terjedő betegségekben;
A terhesség mesterséges megszakítása az abortusz utáni időszak bonyolult lefolyásával;
VAL VEL spontán megszakítás terhesség a történelem során bármikor;
Bonyolult tanfolyammal szülés utáni időszak korábbi születések után;
A nemi szervek fertőző és gyulladásos betegségeivel (colpitis, bakteriális vaginosis) terhesség alatt;
C isthmic-cervicalis elégtelenség;
A polihidramnion vagy a magzati placenta elégtelenség klinikai tüneteivel.
A második szakasz egy átfogó ultrahang vizsgálat azonosítja a méhen belüli fertőzések echográfiai markereit, valamint a magzati placenta elégtelenség jeleit, és felméri annak súlyosságát.
Az IUI-t jelző ultrahangos jelek a következő csoportokba sorolhatók.
1. Az amnion és a chorion patológiája: - polyhydramnion vagy oligohydramnion (a terhesség első trimeszterének végétől diagnosztizálható);
Hyperechoic szuszpenzió a magzatvízben;
Magzatvíz szalagok;
A bolyhos chorion patológiája - a bolyhok hipopláziája (terhesség alatt 8-9 hétig diagnosztizálható, és a chorion elvékonyodásával a teljes kerület mentén 1-3 mm-ig, echogenitásának, folytonossági zavarának és simaságának csökkenésében nyilvánul meg a külső kontúr);
Placentitis, melynek jelei az ödéma/megvastagodás (71,8%), a placenta parenchyma heterogén echogenitása, a bazális lemez kontúrjának megvastagodása/megkettőződése, a lebenyek határainak elmosódása, az intervillous terek és a szubchorionális terek egyenetlen kiterjedése ;
A placenta korai érése.
2. Hasi és szubkután ödéma:
Nem immunhiányos vízkór (szubkután ödéma és pleurális és/vagy szívburok folyadékgyülem vagy ascites);
Hydrothorax;
Kétoldali pleurális folyadékgyülem.
3. Meszesedések a magzat belső szerveiben:
A periventrikuláris régió meszesedése;
bél meszesedések;
Parenchymás máj/lép meszesedések.
4. Az echogenitás változása belső szervek magzat:
Hyperechoiás bél (egy jele van diagnosztikai érték 16 hetes terhesség után);
Bél pneumatosis (az esetek 25%-ában IUI-val észlelve);
Gázbuborékok az epehólyagban;
Hyperechoic nagy vesék normál méretek Hólyag;
A tüdő echogenitásának kétoldali növekedése (enyhe pleurális folyadékgyülem és polyhydramnion kombinációja az intrauterin tüdőgyulladás jele).
5. Szerkezeti hibák (a magzat belső szerveinek fejlődési rendellenességei).
6. Hepatomegalia és splenomegalia.
Az IUI echográfiai markereinek kimutatása nem szolgálhat a diagnózis alapjául. Megjegyeztük, hogy három vagy több echográfiai jel kombinációjával az újszülött méhen belüli fertőzésének valószínűsége eléri a 80% -ot.
A fetometriai paraméterek értékelésekor a magzati növekedési retardációs szindróma (FGR) diagnózisát és formáját határozzák meg. A magzati placenta komplex ereiben végzett véráramlás Doppler-vizsgálata lehetővé teszi olyan rendellenességek kimutatását, amelyek az IUI-ban elsősorban a magzat-placenta véráramlásban mutathatók ki. A kardiotokográfiás vizsgálat lehetővé teszi a kialakuló magzati hipoxia jeleinek diagnosztizálását.
Párhuzamos ultrahang diagnosztika végezzen átfogó vizsgálatot a modern laboratóriumi módszerek kutatás a fertőző betegségek kórokozóinak azonosítására a női szervezetben.
1. Enzim immunoassay egy adott fertőzésre specifikus IgM és IgG vagy a megfelelő kórokozók antigénjeinek meghatározásán alapul.
2. Molekuláris hibridizációs módszer (patogén sejtek DNS- vagy RNS-fragmenseinek azonosítása).
3. ELISA módszer (monoklonális antitestek meghatározása testnedvekben és táptalajokban tesztrendszerrel).
4. A húgycsőből származó natív és Gram-festett kenetek bakterioszkópos vizsgálata, nyaki csatornaés hüvely.
5. Bakteriológiai vizsgálat a méhnyakcsatorna, a húgycső és a hüvely tartalmának folyékony és szilárd táptalajra vetésével, az aerob és anaerob fertőzések képviselőinek és antibakteriális gyógyszerekkel szembeni érzékenységük számszerűsítésére.
6. A méhnyakcsatornából származó kaparék vizsgálata polimeráz láncreakcióval a szexuális úton terjedő betegségek kórokozóinak azonosítására.
A harmadik szakasz A közvetett diagnosztikai módszerek alkalmazása és az intrauterin fertőzés jelenlétét jelző adatok beszerzése után lehetőség nyílik az IUI közvetlen diagnosztizálására szolgáló módszerek alkalmazására a chorionbolholy-biopsziából, amniocentézisből és kordocentézisből nyert anyagban.
A méhen belüli fertőzések diagnosztizálására I trimeszterben terhesség a legkényelmesebb aspirációs transzcervikális chorionboholy biopszia. A terhesség 6-10 hetében készült, ultrahangos szkennelés ellenőrzése mellett. A kapott biopsziás mintát bakteriológiai és virológiai vizsgálatoknak vetik alá, valamint kariotipizálást is végeznek. Nál nél
méhen belüli fertőzés kimutatása esetén fel kell vetni a terhesség megszakításának kérdését, mivel a fertőzéshez in korai időpontok magzati fejlődési rendellenességek kialakulása jellemzi.
A terhesség 16. hetétől és végig II trimeszter méhen belüli fertőzés diagnosztizálására használják amniocentézis. A műtétet aszeptikus körülmények között végezzük transzvaginálisan (az elülső ill hátsó fornix vaginális vagy transzcervikális) vagy transzabdominális hozzáférés (gyakrabban használják). Az ultrahangos szkennelés irányítása alatt a magzatvíz üregének szúrását végezzük a köldökzsinór hurkoktól és a magzat kis részeitől mentes magzatvíz zsebében. A vizsgálathoz három magzatvíz mintát vesznek, összesen 24 ml térfogatban, amelyeket ezt követően mikrobiológiai, biokémiai és genetikai vizsgálatoknak vetnek alá.
Számos teszt létezik a méhen belüli fertőzések kimutatására a magzatvízben: gáz-folyadék kromatográfia magzatvíz a jelenlétre jellemző szerves savak (acetát, szukcinát, butirát, oxálacetát stb.) meghatározására fertőző ágensek a magzatvízben.
A magzatvíz natív és Gram-festett keneteinek bakterioszkópiáját is használják, folyékony és szilárd táptalajra vetve. Az etiológiailag jelentős mikroorganizmusok kimutatása a tenyészetben 5 × 10 2 CFU / ml-t meghaladó mennyiségben diagnosztikai kritérium méhen belüli fertőzés.
A vírusos méhen belüli fertőzések diagnosztizálásában a vírusos ágensek csirkeembriókon történő tenyésztését és a polimeráz láncreakciót alkalmazzák.
Fontos szerepet kapnak a szerológiai kutatási módszerek, amelyek közül a legérzékenyebb és legspecifikusabb a monoklonális antitestek ELISA tesztrendszerrel történő meghatározása.
A tevékenység meghatározása folyamatban van alkalikus foszfatáz köldökzsinórvér leukociták, a vérlemezkék számának számlálása (a thrombocytopenia 150-10 9/l alatt a fertőzés jelének számít), a fiatal leukociták és neutrofilek aránya, valamint a β-laktamáz radioizotóp meghatározása (tipikus β-fertőzés esetén). laktamáz termelő mikroorganizmusok). A vért bakteriológiai, virológiai és immunológiai vizsgálatoknak is alávetik.
Az IUI preklinikai diagnózisa elsősorban az újszülöttek célzott mikrobiológiai vizsgálatán (közvetlenül a születés után) és a méhlepény szövettani vizsgálatán alapul olyan terhes nőknél, akiknél fokozott a magzati fertőzés kockázata.
A mikrobiológiai és szövettani módszerekkel ellentétben az újszülöttek születéskori immunológiai vizsgálata, különösen a köldökzsinórvérben található immunglobulinok főbb osztályainak meghatározása nem kellően informatív az IUI preklinikai diagnózisához. Ez annak a ténynek köszönhető, hogy a G, M, A immunglobulinok azonos értékeit rögzítik újszülötteknél a fertőzés klinikai megnyilvánulásaival és anélkül. A köldökzsinórvérben megemelkedett IgM szint a születés előtti időszakban lezajlott antigén-stimulációt is tükrözi, de nem mindig jelzi a fertőző folyamat jelenlétét.
A méhen belüli fertőzések EGYEDI NOSZOLÓGIAI FORMÁI JELLEMZŐI
Citomegalovírus
A citomegalovírus (CMV) - a herpeszvírusok családjába tartozó DNS-tartalmú vírus, mindenütt jelen van, és különféle testváladékokkal (vérrel, vizelettel), de leggyakrabban szexuális úton terjedhet. Felnőtteknél a fertőzés általában nyilvánvaló klinikai megnyilvánulások nélkül megy végbe, de mononukleózisszerű lefolyása is lehetséges.
A CMV-fertőzés a fertőzött személlyel való szoros érintkezés során vagy az anyától a gyermekig terjedő fertőzés útján fordul elő. A vírus időnként nyálban, vizeletben és nemi szervek váladékában ürül, és csókolózás, szexuális kapcsolat vagy egyéb érintkezés útján terjed.
A citomegalovírus, miután egyszer bekerült az emberi szervezetbe, az elsődleges fertőzés után nem távozik a külső környezetbe, hanem egy életen át megmarad benne. A fertőzés hosszú távú látens lefolyását elősegíti a vírus intracelluláris létezése, ahol megbízhatóan védve van a specifikus antitestek hatásától. Az Oroszországban végzett szerológiai vizsgálatok kimutatták, hogy a terhes nők 90%-a rendelkezik CMV-ellenes antitestekkel, ami rendkívül magas
com vírushordozó szintje. A terhesség alatt valós feltételek teremtődnek a fertőzés újraaktiválásához, amely az immunrendszer működésének terhességi sajátosságaihoz (fiziológiás immunszuppresszió állapotához) kapcsolódik.
A látens fertőzési lefolyású magzat méhen belüli fertőzésének valószínűsége gyakorlatilag hiányzik, reaktiválásával 0,5-7%, elsődleges fertőzés esetén pedig meghaladja a 40%-ot. A prenatális CMV-fertőzés összesített előfordulása 5-20/1000 élveszületett. A cytomegalovírus prenatális fertőzése a szeropozitív nőknél 5%, a fertőzések 20%-a szülés közben következik be, a gyermekek további 10%-a pedig a korai posztnatális időszakban szerez fertőzést - leggyakrabban az anyától, a szennyezett anyatejjel.
A fertőzés leggyakrabban transzplacentális úton halad, ritkábban a magzat lenyeli a fertőzött magzatvizet placentitis és chorioamnionitis jelenlétében.
A vírus a magzat bármely szervét megfertőzheti, beleértve a központi idegrendszert is. A hámsejtek fertőzését nagyméretű intranukleáris zárványok (citomegaliás zárványok) kialakulása jellemzi. Az érintett szövetekben citolízis figyelhető meg fokális nekrózissal és túlnyomórészt mononukleáris területekkel. gyulladásos reakció. A gyógyulás fibrózishoz és meszesedéshez vezet, különösen az agykamrák szubependimális membránjában és a májban. nehéz agyi szövődmények, beleértve a mikrokefáliát és a meszesedést is, általában a méhen belüli fertőzés következményei a terhesség első 3-4 hónapjában, amikor a kamrai rendszer fejlesztés alatt áll.
A terhesség korai szakaszában bekövetkezett vereséggel kapcsolatban embriopátiák alakulnak ki, súlyos trofikus rendellenességek alakulnak ki terhességi zsák, az embrió vagy a magzat elhalása következik be, a terhesség vetéléssel végződik. A halvaszületett magzatokat súlyos agyi rendellenességek jellemzik, beleértve a mikrokefáliát, a vízfejűséget és a meszesedést, a porencephaliát, a hasnyálmirigy cystofibrosisát, a májcirrózist, az epeutak atresiáját, a vesék corticalis diszpláziáját.
A későbbi periódusokban magzati placenta elégtelenséggel járó fetopathiák, intrauterin növekedési retardáció és dysembryogenesis stigmák alakulnak ki. Az újszülötteknél hámsérülések vannak nyálmirigyek, csavarodott tubulusok a vese, hörgők, epe
csatornák. Átfogó (szonográfiás, dopplerometriás és kardiotokográfiás) vizsgálat (hormonok - placenta laktogén, progeszteron, ösztriol, kortizol; AFP tartalom) szerint 33,9%-ban találhatók méhen belüli magzati szenvedés jelei.
Klinikai megnyilvánulások. A méhen belüli CMV-vel fertőzött csecsemők 90-95%-ának születéskor nincsenek tünetei. Legtöbbjük normálisan fejlődik, de a hosszú időn át tartó szoros követés azt jelzi, hogy a gyermekek 10-30%-ánál utólag jelentkeznek kisebb neurológiai károsodás tünetei - idegsüketség, megkésett fejlődés vagy enyhe szellemi retardáció. Ezenkívül lehetséges a celluláris immunitás funkciójának specifikus megsértése - a T-segítők aktivitásának gátlása, az IgM és az IgG tartalmának növekedése.
A fertőzés klinikai tüneteit mutató gyermekek kis hányadánál ezek a méhen belüli késleltetés növekedés (leggyakrabban a máj és a lép növekedéseként) vagy egy külön szerv folyamatában való érintettség súlyos, generalizált, életveszélyes betegség, ami ritka.
A veleszületett citomegalovírus fertőzés számos extragenitális megnyilvánulása (hepatitis, thrombocytopenia, hemolitikus anémiaés tüdőgyulladás) kezelés nélkül bizonyos időn belül eltűnnek. A neurológiai károsodás visszafordíthatatlan, bár a rokkantság mértéke változó. A legtöbb veleszületett gyermek citomegalovírus fertőzés Az idegrendszeri károsodás tüneteivel született gyermekek súlyos, visszafordíthatatlan neurológiai rendellenességekben szenvednek, beleértve az agyi bénulást, az epilepsziát és az idegi süketséget. A chorioretinopathia meglehetősen gyakori. Ritkán okoz látászavart, és kényelmes diagnosztikai eszköz a veleszületett fertőzések gyanúja esetén, bár nem különböztethető meg a toxoplazmózis okozta chorioretinopathiától. A veleszületett citomegalia mortalitása 20-30%.
Megelőzés és kezelés. A mai napig nem fejlesztettek ki hatékony, biztonságos vakcinákat vagy kész specifikus monoklonális antitestek készítményeit. A megelőző intézkedések a fertőzött újszülöttek elkülönítésére és a szeronegatív terhes nőkkel való érintkezés kizárására korlátozódnak. Az őket gondozó személyzet kesztyűben és egy másodpercben dolgozik
fürdőköpeny. Passzív profilaxisként használhatja a kész antitestek készítményeinek bevezetését magas tartalom anticytomegalovírus IgG.
Az α-herpesvírusok (herpes simplex vírus és varicella-zoster vírus) által okozott fertőzések kezelésében elért közelmúltbeli előrelépések ellenére a β-herpesvírusos betegségek kezelését nem fejlesztették ki véglegesen. Valaciklovirt és ganciklovirt alkalmaznak, de terhes nőkön történő alkalmazásukkal kapcsolatban nincs elegendő tapasztalat. A kezelési komplexum magában foglalja a növényi adaptogének (eleutherococcus, ginzeng, méhpempő), a B csoportba tartozó vitaminok (B 1, B 6, B 12) alkalmazását a terhesség 14 hetéig.
15-16 héttől kezdődően a palliatív kezelés módszereként immunglobulin-terápiát végeznek normál humán immunglobulinnal vagy kész antitest-készítményekkel, amelyek magas citomegalovírus-IgG - anti-citomegalovírus immunglobulin-tartalommal rendelkeznek. Az immunglobulin készítmények bevezetésével az anya szervezete kész antitesteket (AT) kap a CMV ellen. Az IgG osztályú abs aktívan áthaladnak a placentán, és passzív immunitást hoznak létre a magzatban. A terhes AT szervezetében blokkolják az extracellulárisan elhelyezkedő vírusokat, immunkomplexeket hoznak létre velük, elősegítik a szervezetből való kiürülést, korlátozzák terjedésüket a nyirok- és vérkeringésben. Az immunglobulin terápia során figyelembe kell venni az allergiás, pirogén reakciók kockázatát, az anti-y-globulinok termelődését, a fertőzés súlyosbodását, i.e. olyan helyzetekben, ahol nagyobb a fertőzés káros hatásainak kockázata.
A leukociták csökkent α- és y-interferon-termelő képességére vonatkozó adatok vírusfertőzésben szenvedő nőknél azt mutatják, hogy tanácsos immunmoduláló és interferonkorrekciós összetevőket bevonni a citomegalovírus fertőzésben szenvedő terhes nők komplex terápiájába. Egy genetikailag módosított rekombináns gyógyszer viferont használnak, amely egy antioxidánsokhoz kapcsolódó a2-interferon. Interferonstabilizáló, immunmoduláló és antioxidáns tulajdonságokkal rendelkezik.
A herpeszfertőzések kezelésében újdonság a plazmaferezis és az endovaszkuláris lézeres vérbesugárzás (ELOK) alkalmazása. A plazmaferezis és az ELOK terápiás hatékonysága a méregtelenítő hatásnak köszönhető, serkentő hatás
sejtes és humorális immunitásés a nem specifikus rezisztencia reakciói, a vér koagulációs és aggregációs tulajdonságainak normalizálása.
herpetikus fertőzés
A legfontosabb szerepet a család vírusai játsszák herpesviridae. A herpes simplex vírus (HSV) DNS-tartalmú, és a CMV-vel azonos csoportba tartozik. Epstein-Barr vírusés vírus bárányhimlő- övsömör. Két szerotípusát, a HSV-1-et (orolaabiális) és a HSV-2-t (genitális) azonosították, de nincs teljes megfelelés a szerotípus és a fertőzés lokalizációja között. Az újszülöttkori fertőzések 20%-ában genitális HSV-1 fertőzéssel társul.
A herpes simplex vírust továbbítják különböző utak, a legfontosabb a szexuális út. A genitális herpesz vírus vereségét a terhes nők 7% -ánál észlelik. Az újszülötteknél a herpesz gyakorisága 1:2000-1:5000, de az újszülöttkori herpesz viszonylagos ritkasága ellenére megnyilvánulásainak súlyossága és az újszülött számára kedvezőtlen prognózis nagyon fontossá teszi a diagnózis ésszerű megközelítését. , ennek a rendkívül súlyos betegségnek a kezelése és különösen a megelőzése.
A HSV-2 kimutatásának gyakorisága számos tényezőtől (életkor, szexuális aktivitás jellege, a lakosság szociokulturális szintje stb.) függően jelentősen változik. Így a 15 év alatti serdülőknél a szeropozitív eredmények kevesebb, mint 1%, míg a nemi betegségekre szakosodott klinikák betegei között 46-57%. Terhes nőknél a HSV-2 elleni specifikus antitesteket, például az USA-ban, átlagosan a nők 20-30%-ánál mutatják ki.
Az anya elsődleges fertőzésének klinikai megnyilvánulásai 18-22 napig tartanak, a tünetek az 1. héten fokozódnak. A következő 2 hétben a vírus által károsított hám tünetmentes hámlása figyelhető meg. A megnyilvánulások teljes időtartama közel 6 hét. A nem elsődleges genitális fertőzés kevésbé kifejezett: a klinikai megnyilvánulások időtartama rövidebb (kb. 15 nap), ritkább a vírus tünetmentes ürítése, időtartama 8 napra csökken. A relapszusok klinikai megnyilvánulásainak súlyossága és időtartama még kevésbé kifejezett, és a sérült hám hámlási időtartama mindössze 4 nap.
Elsődleges genitális herpesz az anyában és súlyosbodása krónikus folyamat a legveszélyesebbek a magzatra. Ha az újszülöttek 0,5-1,0%-a intranatálisan fertőzött, akkor azzal akut lefolyás vagy exacerbáció, amely a bőr és a nemi szervek nyálkahártyájának hólyagos elváltozásaiban nyilvánul meg, a magzat szülés közbeni fertőzésének kockázata eléri a 40%-ot.
Méhen belüli HSV-2 fertőzés esetén a legtöbb esetben a magzat fertőzése közvetlenül a szülés előtt, a membránszakadás után felszállóan (kritikus periódus 4-6 óra) vagy szülés közben, fertőzötten áthaladva következik be. szülőcsatorna(85%). A fertőzés terjedése a méhnyak és a szeméremtest elváltozásainak jelenlétében és a vírus tünetmentes izolálása esetén is előfordul. A fertőzés emelkedő útján a kórokozó szaporodik és felhalmozódik a magzatvízben, polihidramnion figyelhető meg. A fertőzés megtörténte után a vírus kontakt vagy hematogén úton terjedhet. 5%-ában transzplacentális terjedés történik terhesség alatt.
A méhlepény és a magzat herpeszfertőzéssel járó veresége a terhesség bármely szakaszában előfordulhat, és a magzat kialakulásához vezethet születési rendellenességek fejlődés, születés előtti halál, vetélés vagy koraszülés. Az első trimeszterben bekövetkezett fertőzés vízfejűség kialakulásához, szívhibákhoz, a gyomor-bél traktus anomáliáihoz, gyakran előfordul spontán vetélés, és méhen belüli növekedési retardáció alakul ki. II és III trimeszterben fertőző folyamat hepatospelenomegalia, vérszegénység, sárgaság, tüdőgyulladás, meningoencephalitis, szepszis, alultápláltság kialakulásához vezet. Az intrauterin fertőzés a terhesség késői szakaszában nyilvánul meg korai fejlesztésújszülöttkori fertőzés klinikai képe (első nap) akár ennek következtében született gyermekeknél császármetszés. A herpetikus fertőzés gyakori megnyilvánulásai: bőr-, szájnyálkahártya-károsodás, chorioretinitis.
Az újszülöttkori herpeszvírus fertőzés három klinikai formában nyilvánul meg.
Helyi forma a bőr és a nyálkahártyák elváltozásaival- 45%. A bőr és a nyálkahártya károsodása a leggyakoribb, de egyben a legtöbb is könnyű formaújszülöttkori herpesz. Szem: keratoconjunctivitis és chorioretinitis. Bőr és szájnyálkahártya: hólyagok,
bőrpír, petechiák. Ha nem kezelik, a betegség súlyos szövődmények kialakulásával előrehaladhat. A halálozás körülbelül 18%.
Helyi forma központi idegrendszeri károsodással(encephalitis) - 35%. Jellemzők: láz, letargia, étvágycsökkenés, depresszió vagy izgatottság szindróma, remegés, görcsök. Az agy-gerincvelői folyadékban jelentős változásokat találnak. A halálozás terápia hiányában több mint 50%.
Terjesztett forma- húsz%. Az újszülöttkori herpesz disszeminált formájával általában több szerv is részt vesz a folyamatban egyszerre: a máj, a tüdő, a bőr, a mellékvesék. A tünetek az 1.-2. élethéten jelentkeznek, ide tartoznak a lokalizált formájú tünetek, étvágytalansággal kombinálva, hányás, levertség, láz, sárgaság, légzési zavarok, vérzés, sokk (35. ábra). A vérzés és az erek összeomlása hirtelen és gyorsan végzetes lehet. A halálozás ebben a formában rendkívül magas - 90%. A modern antiherpetikus kemoterápia jelentősen javíthatja a prognózist, de a folyamatos kezelés ellenére továbbra is meglehetősen magas a hosszú távú neurológiai rendellenességek kockázata.
A jövőben túlélő gyermekeknek súlyos szövődményei vannak (neurológiai rendellenességek, látáskárosodás, pszichomotoros retardáció).
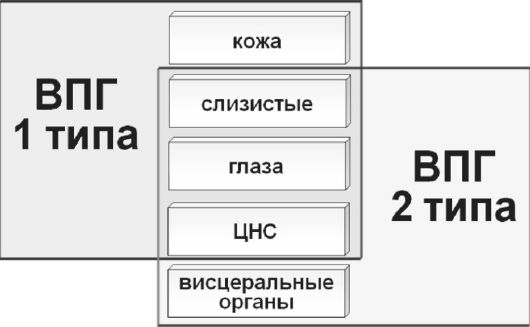 Rizs. 35. A herpeszvírusok szöveti tropizmusa
Rizs. 35. A herpeszvírusok szöveti tropizmusa
Terhesség megelőzése, kezelése és kezelése. A természete a megelőző és orvosi intézkedések, valamint a szülészeti taktika típusától, formájától (tipikus, atipikus, tünetmentes és a tanfolyam időtartamától) és a nemi szervek elváltozásainak meglététől, a membránok állapotától függ.
A terhesség korai szakaszában jelentkező elsődleges fertőzés esetén fel kell vetni annak megszakításának kérdését. Ha a betegség későn jelentkezik, vagy a nő a terhesség előtt fertőzött, a megelőző intézkedések közé tartozik a magzat fejlődésének és állapotának dinamikus echográfiás monitorozása, terápiás kurzusok előírása, beleértve a metabolikus komplexet, a sejtmembrán-stabilizátorokat, az unitiolt. A terhesség megszakításának kérdése egyénileg dönt.
Bizonyított előny komplex kezelés herpetikus elváltozások. A fő kemoterápia az acyclovir vagy valaciclovir. A kemoterápia a terhesség első trimeszterétől lehetséges. Annak ellenére, hogy nincs bizonyíték a teratogén és embriotoxikus hatásra, az acyclovir terhes nők számára történő kijelölése korlátozott a a következő jelzéseket: elsődleges genitális herpesz, visszatérő genitális herpesz (tipikus forma), nemi herpesz vetélés veszélyével vagy IUI tüneteivel kombinálva. Azoknál a terhes nőknél, akiknél a fertőzés gyakran kiújul, állandó acyclovir-kezelést (szuppresszív terápia) végeznek. A herpeszfertőzés bonyolult lefolyása (tüdőgyulladás, agyvelőgyulladás, hepatitis, koagulopátia) esetén a kezelést fertőző szakorvossal közösen végzik.
Ugyanakkor célszerű immunglobulin terápiát, interferon készítményeket, "nagy" antioxidánsokat (E és C vitamin) felírni. Meg kell jegyezni a herpeszhez kapcsolódó betegségek (leggyakrabban chlamydia, mycoplasmosis, trichomoniasis, candidiasis, bakteriális vaginosis) kezelésének szükségességét. A cytomegalia kezelésén túl a plazmaferezis és az endovaszkuláris lézeres vérbesugárzás is megállta a helyét a herpeszfertőzés kezelésében. Komplex terápia után az anya és a magzat szövődményeinek gyakorisága 2-3-szorosára csökken.
A genitális herpeszben szenvedő nők szülészeti kezelése a terhesség formájától és időtartamától függ. Terhesség alatti primer fertőzés (1 hónappal a szülés előtt vagy kevesebb) vagy kiújulása esetén (néhány nappal a szülés előtt) kemoterápiát végeznek,
a szülés császármetszéssel történik. Ha az egyik szülőnél előfordult genitális herpesz, a szülés előtt tenyésztési vizsgálat vagy PCR szükséges. Ha a válasz nemleges - szállítás a szülőcsatornán keresztül.
A megfelelően szervezett szülészeti ellátás ellenére jelenleg nincsenek feltételek a HSV-fertőzés anyáról újszülöttre való átvitelének teljes megszüntetésére. Ez annak köszönhető, hogy nem lehet minden nőt azonosítani, akiknek tünetmentes genitális herpesz fertőzése van. Ebben a tekintetben a herpeszfertőzés újszülöttekre történő átadásának 70% -ában pontosan a tünetmentes herpeszben szenvedő anyáktól származik.
Rubeola
A rubeolavírus szerepét a veleszületett fejlődési rendellenességek kiváltó okaként Norman Gregg ausztrál szemész ismerte fel először 1941-ben. Először írt le szürkehályog, süketség és veleszületett szívbetegség szindrómáját olyan gyermekeknél, akiknek anyja terhessége alatt rubeolában szenvedett az 1940-es sydneyi járvány idején. A vírust először 1962-ben izolálták szövettenyészetben. 1969-re megjelent egy hatékony élő, gyengített vakcina.
A rubeolavírus RNS-tartalmú vírus, és a togavírusok (mikrovírusok) csoportjába tartozik. Az ember az egyetlen hordozó. A rubeola vírus nem ellenálló külső környezet, levegőben lévő cseppekkel terjed, a fertőzéshez hosszan tartó érintkezés szükséges, egyetlen érintkezés általában nem elegendő, de mivel a betegség gyakran tünetmentes, előfordulhat, hogy nem ismerjük az érintkezést.
A rubeolában átesettek túlnyomó többségében stabil immunitás alakul ki, azonban az emberek 0,3-4,25%-a ismét rubeolát kap, mivel a meglévő humorális immunitás gyengébbsége miatt lehetséges a korábban átvitt rubeola újraaktiválása, illetve az újrafertőződés. Ugyanakkor a szentpétervári kutatók szerint a gyakorlatban ilyen megfigyelések valójában nem fordulnak elő, és ha klinikailag és szerológiailag kizárják az akut rubeolát, akkor az intrauterin fertőzés kockázata kizárt. Ha a rubeola antigén elleni antitestek titere magas vagy növekszik, akkor az anyában kell meghatározni a specifikus IgM antitesteket, és ha kimutatják, a kordocentézissel nyert magzati vérben.
A magzat fertőzése csak beteg anyától származik. A rubeolában szenvedő nőknek a gyógyulás után legkorábban 6 hónappal javasolható a terhesség. A vereség a virémia és a vírus transzplacentális behatolása következtében következik be.
A klinikai tünetek önmagukban nem elegendőek a diagnózis felállításához. Ugyanebből az okból kifolyólag az anamnézisben szereplő rubeola nem utal immunitásra. A rubeola fertőzés bizonyításához vírusizoláció vagy megfelelő szerológiai vizsgálat szükséges.
A közelmúltban előforduló rubeola diagnózisának kritériumai a következők:
A rubeola vírus izolálása (általában a torokból);
Az antitesttiter 4-szeres vagy nagyobb növekedése;
Rubeola-specifikus IgM jelenléte, amelyet csak az elsődleges fertőzést követő 4-6 héten belül határoznak meg.
Ha a diagnózis továbbra is kétséges, különösen, ha a kontaktus a terhesség legkorábbi szakaszában történt, a 14-20. héten amniocentézis végezhető, és megkísérelhető a rubeola vírus izolálása a magzatvízből, amely sikeressége esetén legalább a placenta fertőzése. A negatív tenyésztési eredmények nem zárják ki a placenta vagy a magzat fertőzését. A legpontosabb a kordocentézis.
A rubeola terhes nőknél a következő következményekkel járhat:
Nincs hatással a magzatra;
Csak a placenta fertőzése;
A méhlepény és a magzat fertőzése (tól tünetmentes lefolyás sok rendszer veresége előtt);
Magzati halál (a terhesség spontán idő előtti megszakadása vagy halvaszületés).
A magzati fertőzés a terhesség bármely szakaszában követheti az anyai fertőzést, a rubeola kimenetele nagymértékben függ a terhességi kortól.
A magzat fertőzésének valószínűsége a terhesség 8 hete előtt 54%, 9-12 héten - 34%, 13-24 héten - 10-20% és legfeljebb 12% - a második trimeszter végétől számítva. A terhesség első 8 hetében jelentkező virémia a méhlepény fertőzéséhez és spontán vetélés vagy halvaszületés; ha a terhesség közepén fertőződik, a rubeolaris fetopathiát gyakrabban diagnosztizálják koraszülötteknél; rubeola fertőzéssel a harmadik trimeszterben
veleszületett fejlődési rendellenességek, például krónikus encephalitis és produktív leptomeningitis nélkül megy végbe újszülötteknél.
Veleszületett rubeola klinikája. A rubeolavírus kivételes tropizmust mutat a fiatal embrionális szövetek tekintetében, ami ebben a betegségben embriopátiával jár. A magzatot sokféleképpen érinti a rubeola vírus. Kioszt "klasszikus veleszületett rubeola szindróma" amely a legjellemzőbb fejlődési rendellenességek hármasát tartalmazza: szürkehályog a szaruhártya elhomályosodásával, szívhibák(a kamrai septum veleszületett rendellenességei - rubeoláris embriopátia) és süketség(vérzések lágy szövetek külső, középső és belső fül). A veleszületett rubeola szindrómát gyakran kombinálják produktív intersticiális tüdőgyulladással, az alveolociták óriássejtes metamorfózisával.
A klasszikus mellett van "Előrehaladott veleszületett rubeola szindróma" amely a három nevezett malformáción kívül számos egyéb fejlődési rendellenességet is tartalmaz: mikrokefália, megnagyobbodott fontanelle, agykárosodás, zöldhályog, szájpadhasadék, intersticiális tüdőgyulladás, hepatitis, vesztibuláris apparátus károsodása, csontváz rendellenességek, tubuláris csontok károsodása, hepatosplenomegalia, genitourináris rendellenességek szervek.
A születéskor szerológiailag fertőzött túlélő gyermekek 70%-a egészséges, de életük első 5 évében a gyermekek több mint 2/3-ánál jelentkeznek fertőzésre utaló jelek. Leggyakrabban ezek kevésbé nyilvánvaló szövődmények, amelyek enyhe vagy közepes süketségből és agykárosodásból állnak, késleltetett pszichomotoros fejlődéssel. A rubeola késői megnyilvánulásai közé tartoznak az immunológiai diszkráziák (az újszülött vírusfertőzésre adott válaszként saját immunglobulinok szintézisének késése), halláskárosodás, pszichomotoros retardáció, autizmus, agyi szindrómák (szklerotizáló panencephalitis), diabetes mellitus.
A rubeola újszülöttkori megnyilvánulásai közül a thrombocytopeniás purpura a legjellemzőbb, amely 2 héttől 3 hónapig tart. Tipikus hepatitis sárgasággal, hemolitikus vérszegénység retikulocitózissal és deformált vörösvértestekkel, az elülső fontanelle bezáródása agy-gerincvelői folyadék pleocitózisával, intersticiális tüdőgyulladás, a tubuláris csontok károsodása (röntgenvizsgálattal kimutatható, és váltakozó tömörülési és csontritkulási területekből áll). A szívhibák közül a leggyakoribb
az artériás (Botallov) csatorna hasadéka, gyakran szűkülettel kombinálva pulmonalis artéria. Vannak még az aorta szűkülete és koarktációja, VSD és ASD, nagy erek transzpozíciója; a "kék" típusú hibák ritkák.
A legtipikusabb szembetegség - a szürkehályog - a rubeola vírus közvetlen hatásának eredménye, amely több évig is megmaradhat a lencsében. A szürkehályog születéskor hiányozhat, és az újszülöttkori időszakban jelentkezhet. A glaukóma 10-szer ritkábban fordul elő. Ezenkívül rubeola esetén pigmentált retinopátia, szaruhártya elhomályosodás, rövidlátás és a szemhéjak fejletlensége észlelhető.
A veleszületett rubeola leggyakoribb hibája a süketség, amelyet gyakran vestibulopathiával kombinálnak - ez a Corti-szerv hibája.
Minél rövidebb terhességi korban kapnak rubeolát a nők, annál gyakrabban nyilvánul meg a vírus teratogén hatása. A rubeola teratogén veszélye a terhesség első hónapjában 35-50% (egyes jelentések szerint megközelíti a 100%), a 2. hónapban -
25%, a 3. - 7-10%.
A rubeola magzatra gyakorolt káros hatása nemcsak teratogén hatásában nyilvánul meg. rubeola fertőzés be korai időszak a terhesség 10-40%-ában spontán vetéléshez, 20%-ban halvaszületéshez vezethet, az élve született gyermekek 10-25%-a meghal az újszülött korban.
A rubeola-betegség a terhesség első trimeszterében, amelyet klinikai, epidemiológiai és laboratóriumi adatok is megerősítenek, a terhesség megszakításának indikációja. Ha terhes nő rubeolában szenvedő beteggel érintkezik, legkésőbb 10-12 napon belül szerológiai vizsgálatot kell végezni. Ha a szeronegatív reakció továbbra is fennáll, szoros megfigyelés és 2 hét múlva ismételt szerológiai vizsgálat a tünetmentes fertőzés kimutatása érdekében.
A megelőzés elsősorban immunizálással történik. A gyermekek oltása kötelező. A terhes nőket nem oltják be, mert gyengített vakcinát alkalmaznak. élő vakcinaés a teratogén hatás nem zárható ki. Fogamzóképes korú nőknél javasolt a rubeolavírus antigénjei elleni antitestek szűrése.
Toxoplazmózis
Toxoplasma gondii a protozoonhoz tartozik, amely szinte bármilyen típusú sejtet megfertőz emlősökben. Ez a fertőző ágens az egész világon elterjedt, embereket és állatokat érint, de a szaporodás végső ciklusa csak a macskafélék beleiben fordul elő. Az oociszták a talajból kerülnek be annak a személynek a szervezetébe, aki zöldséget vagy más, oocisztákkal szennyezett élelmiszert eszik. Az oociszták bélben történő felszívódását követően trophozoiták szabadulnak fel. Behatolnak a hámba, ahol elszaporodnak, majd - a nyirok- és keringési rendszeren keresztül - szétterjednek az egész szervezetben. Az egészséges immunkompetens gazdaszervezetben a trofozoiták szaporodását a sejtes immunválasz kialakulása és kisebb mértékben a specifikus antitestek termelése korlátozza. Ezen organizmusok egy része megakadályozza a szöveti pszeudociszták képződését, amelyek intersticiális védőburokkal körülvett organizmusok felhalmozódása. Ebben a formában látensek maradnak, de életképesek a gazdaszervezet egész életében, általában anélkül, hogy jelentős immunválaszt okoznának. Ha a normál immunitás valamilyen okból csökken, a fertőzés újra aktiválódhat.
A fertőzés másik fontos módja a fertőzött állat nyers vagy rosszul főtt húsának elfogyasztása. Ily módon az ember leggyakrabban bárány- vagy sertéshús fogyasztásakor kap fertőzést. A fertőzés nem terjed egyik emberről a másikra, kivéve a méhlepényen keresztül az anyáról a magzatra a fejlődés során. akut fertőzés terhesség alatt. Nincsenek meggyőző adatok a krónikus vagy látens fertőzés és a visszatérő vetélések összefüggéséről.
Az emberi fertőzés gyakorisága T. gondii bármely populációban függ az éghajlattól, az ételkészítés módjától és ezen kívül a macskákkal való érintkezéstől. A kimutatható antitestek prevalenciája folyamatosan nő
A veleszületett toxoplazmózis gyakoriságát nehéz meghatározni, mivel a legtöbb fertőzött gyermek születéskor gyakorlatilag egészséges, és az anya fertőzése általában tünetmentes. Bizonyíték van arra, hogy a legtöbb fertőzött gyermek később szenved súlyos szövődmények ez a fertőzés, amely speciális, hosszú távú kezelést igényelhet. A veleszületett fertőzés elméleti becsült kockázata a fogamzóképes korú nők éves szerokonverziós aránya alapján 4-50/10 000 élveszületett.
A fertőzés klinikai megnyilvánulásai. A toxoplazmózis fertőzésének klinikai megnyilvánulásai a következők.
"Szerzett toxoplazmózis. A legtöbb esetben emberi fertőzés T. gondii tünetmentes vagy fel nem ismert. a legtöbben gyakori megnyilvánulása fertőzés generalizált lymphadenopathia, amely bár nem mindig, de rosszulléttel, lázzal, torokfájással, fejfájással, bőrkiütéssel jár. Néha egyidejűleg atipikus limfocitózist találunk heterofil antitestek nélkül. A fertőzés általában korlátozott. Ritka, súlyosabb esetekben az agy, a szívizom, a máj vagy a tüdő érintett a fertőző folyamatban, ami megköveteli specifikus kezelés. A chorioretinitis viszonylag ritka, és általában egyoldalú. * Veleszületett toxoplazmózis. Ha egy nő toxoplazmózissal fertőzött a terhesség legelején, a magzatra való átvitel kockázata viszonylag kicsi (körülbelül 20%), de ebben az időszakban előfordulhat, hogy a fertőzés megfertőződik. súlyos következményekkel jár a magzat haláláig. Születéskor a veleszületett toxoplazmózisban szenvedő gyermekek mindössze 10-20%-ánál észlelnek rendellenességeket, a legtöbb súlyos betegségben szenvedő gyermek a terhesség korai szakaszában fertőződik meg. A súlyos méhen belüli toxoplazmózis halálhoz vezethet, ill
súlyos anomáliák a magzat fejlődésében, beleértve a vízfejűséget, ciszták képződését meszesedéssel vagy az agykéreg extrém elvékonyodásával, meszesedéssel, gliaburjánzással, produktív endarteritissel, generalizált ödéma kialakulása hidrothoraxszal és ascitessel, kiterjedt gyulladás és szövetpusztulás különböző szervekről. A szülés után krónikus villusitis derül ki, a bolyhok stromájában - limfoid infiltráció plazmasejtek keverékével. konkrét jel a kórokozó kimutatása ciszták vagy szabadon fekvő formák formájában, Romanovsky-Giemsa kenetek-lenyomatok szerint a méhlepény anyai felületéről vagy a méhlepény szövet bevágásának mélységéből; a végső diagnózis a magzati intersticiális pszeudocisztákban lévő protozoák kimutatásán alapul.
Súlyos veleszületett toxoplazmózisújszülötteknél ez gyakran általános betegség, amely vérszegénységben, a máj és a lép megnagyobbodásában, sárgaságban, lázban és limfadenopátiában nyilvánul meg. A szemfenék alapos vizsgálatakor a legtöbb fertőzött gyermeknél a kétoldali chorioretinitis jelei mutatkoznak. A központi idegrendszer érintettsége koponyán belüli meszesedés, görcsrohamok, vízfejűség, mikrokefália vagy cerebrospinális folyadék elváltozások formájában jelentkezhet (különösen haladó szint mókus). A születéskor a toxoplazmózis klinikai tüneteit mutató gyermekek hozzávetőleg 80%-a visszafordíthatatlan agykárosodást szenved, és 50%-a látáskárosodást szenved. Ha az anya a terhesség későbbi szakaszában megbetegszik toxoplazmózisban, akkor a magzat nagyobb valószínűséggel fertőződik meg, de születéskor a fertőzés klinikai jelei többnyire nem jelentkeznek, és ha igen, akkor általában a szemgolyó vagy a központi idegrendszer és az újszülöttben gyakran észrevétlen marad.
A szemtünetek fokozatosan jelentkeznek a fertőzött gyermekek több mint 80%-ánál, bár néha csak idősebb gyermekeknél vagy serdülőknél ismerik fel őket. Ebben a csoportban körülbelül 4 gyermek szenved jelentős látásvesztésben, és ugyanennyien ismétlődő aktív chorioretinitisben, legalább átmeneti látáskárosodással.
komoly Neurológiai rendellenességek ritkább (<10%), в отдаленном периоде прицельное изучение умственных способ-
Az eredmények azt mutatják, hogy több gyermeknél romlik az eredmények. Gyakran előfordul részleges halláskárosodás.
Toxoplazmózisban szenvedő terhes nők megelőzése és kezelése. A toxoplazmózissal való fertőzés kockázata a következő módokon csökkenthető.
1. Kerülje az alulsütött vagy nyers hús, különösen a sertés- vagy bárányhús fogyasztását, és a nyers hús kezelése után alaposan mosson kezet.
2. Nem szükséges elkerülni a házimacskával való érintkezést a terhesség alatt, bár jobb, ha ilyenkor nem kezdünk új állatot. A macskahomokot gyakrabban kell cserélni, lehetőleg valaki másnak. Csak főtt vagy konzerv húst szabad etetni.
3. A friss zöldségeket fogyasztás előtt alaposan meg kell mosni, hogy szennyezett föld ne kerüljön az ételbe.
4. Kertészkedés után alaposan moss kezet, különösen étkezés előtt.
A terhes nők akut toxoplazmózisa és a magzati fertőző folyamat kezdete között jelentős idő telik el. Ha a fertőzés a terhesség első felében alakul ki, akkor felvethető az indukált abortusz kérdése, mivel a magzatra való átterjedésének kockázata a korai szakaszban megközelíti a 20%-ot, és a következmények pusztítóak. A terhesség késői szakaszában a terhes nőt pirimetaminnal, szulfonamidokkal, tindurinnal kezelik. A makrolid antibiotikumot, a spiromicint sikeresen alkalmazták.
Chlamydia
A chlamydia leggyakrabban szexuális úton terjed, és főként a hengeres hám sejtjeit érinti. Az is bebizonyosodott
a chlamydia „hazai” úton történő terjedésének lehetősége, főként kisgyermekek körében.
A chlamydia klinikai megnyilvánulásai. A chlamydia urogenitális traktusba való bejutását nem mindig kísérik észrevehető klinikai megnyilvánulások. A betegség gyakran submanifest vagy tünetmentes. A fertőzött nők felének nincs klinikai megnyilvánulása. A chlamydia urethritisnek nincsenek specifikus megnyilvánulásai, és a betegek ritkán panaszkodnak dysuriára. Néha a chlamydia a csatornák és a Bartholin mirigyek exudatív gyulladását okozhatja. A cervicitis a chlamydia aktivitás elsődleges és leggyakoribb megnyilvánulása. A méhnyakcsatornából származó váladék macerálja a méhnyak hüvelyi részének rétegzett laphámját, ami részleges hámlást okoz. A méhnyak ödémássá, hiperémiássá válik, kialakul az úgynevezett hipertrófiás méhnyak ectopia. A Chlamydia salpingitis a felszálló chlamydia fertőzés leggyakoribb megnyilvánulása. A chlamydia salpingitis és a salpingo-oophoritis jellemzője a hosszú, szubakut, letörölt lefolyás, nem hajlamos a "súlyozásra". A krónikus fertőzés petevezeték elzáródást, méhen kívüli terhességet és meddőséget okozhat. A felszálló chlamydia fertőzésben kismedencei gyulladásos betegségben szenvedő nőknél perihepatitis, a Fitz-Hugh-Ciirtis szindróma alakulhat ki. Ezt a szindrómát láz, fájdalom a májban és a kismedencei szervekben jellemzi.
Az urogenitális chlamydia mellett extragenitális chlamydia fertőzés (ophthalmochlamydia) is lehetséges, míg az ophthalmochlamydiás betegek 72%-ánál az urogenitális traktus chlamydia fertőzése is előfordul.
Az urogenitális chlamydiát terhes nőknél 3-12%-ban diagnosztizálják, eléri a 33-74%-ot a nemi szervek krónikus gyulladásos betegségeiben, krónikus nem specifikus tüdőbetegségekben, súlyosbodott szülészeti anamnézisben (halvaszületés, újszülött méhen belüli tüdőgyulladása, koraszülés, szokásos vetélés) .
A chlamydia terhesség általában komplikációkkal jár. Az első trimeszterben jellemző a terhesség megszakításának veszélye, a nem fejlődő terhesség, a vetélések. A vetélések gyakorisága 25%, a perinatális veszteségek koraszülés esetén - akár 5,5%.
A chlamydia nemcsak szokásos vetéléshez vezet, hanem a magzat és az újszülött méhen belüli fertőzéséhez is. A chlamydia elsősorban a kötőhártyát, a nasopharynxet, a légutakat, a beleket kolonizálja, de a legjellemzőbb az agyhártya és az agyanyag elváltozása, ahol már makroszkóposan meghatározottak a gyapotszerű lerakódások, elsősorban a féltekék felső oldalfelületein. Szövettanilag granulomáknak tűnnek. A chlamydia fertőzés következménye a születés előtti mortalitás növekedése, a trachomaszerű kötőhártya-gyulladás és a tüdőgyulladás előfordulása újszülötteknél. Amikor a magzatvíz membrán fertőződik, polihidramnion alakul ki, a placenta specifikus elváltozása magzati placenta elégtelenség (27%), sdfd és magzati hypoxia kialakulásához vezet. A chlamydia okozta perinatális mortalitás eléri a 15,5%-ot, és a születés utáni időszakban meghalt újszülöttek aránya az összes perinatális veszteség több mint fele.
Klinikai megnyilvánulások. A terhes nők 17-30%-ánál a chlamydia látensen vagy kisebb tünetekkel jelentkezik. Vegyes fertőzés jelenlétében komplett tünetegyüttes lehet, beleértve a cervicitist és a cervicalis ectopiat.
A chlamydia terhes nőknél általában bakteriális és vírusos fertőzéssel párosul, így a magzat fertőzése gyakran ezen kórokozók együttes hatása miatt következik be. Ez az újszülöttben a fertőzés klinikai megnyilvánulásainak polimorfizmusát okozza, ezért a chlamydia fertőzés tipikus megnyilvánulásai mellett (kötőhártya-gyulladás, vulvovaginitis, tüdőgyulladás) vannak olyan formák is, amelyek nem jellemzőek a chlamydiára (vesiculopustulosis, omphalitis, rhinitis, szepszis). .
A chlamydiás anyáktól született újszülöttek méhen belüli fertőző betegségeinek klinikai megnyilvánulásai három csoportra oszthatók: kisebb formák, súlyos formák és az úgynevezett fertőzési szindróma.
A kis formák a következőket tartalmazzák:
kötőhártya-gyulladás;
Vulvovaginitis;
Vesiculopustuloses, rhinitis, otitis media, omphalitis - vegyes fertőzéssel.
A chlamydia fertőzésben szenvedő újszülöttek méhen belüli fertőzésének súlyos formái:
Chlamydia tüdőgyulladás;
Általános gyulladásos folyamat szepszis kialakulásával és számos fertőzési góc jelenlétével (tüdőgyulladás, köldökvéna phlebitis, meningitis, hepatitis) - vegyes fertőzéssel.
A fertőzési szindróma esetén az intrauterin fertőzés helyi és általános megnyilvánulásai hiányoznak. Az újszülötteknél az adaptációs folyamatok megsértése, a bőr elszíneződése, az izomtónus csökkenése, a reflexek instabilitása, az elhúzódó sárgaság, a kezdeti 10% -os vagy annál nagyobb súlyvesztés, lassú felépülése ismételt eséssel.
A chlamydia megelőzése és kezelése terhesség alatt. A chlamydia terhesség alatti kezelése bizonyos nehézségekkel jár, ami összefügg a betegség lefolyásának sajátosságaival, a placenta rendszer egyidejű diszfunkciójával, a magzatra gyakorolt káros hatások lehetőségével a hagyományos kezelési rendekkel.
Antibakteriális terápia a makrolidok csoportjába tartozó gyógyszerekkel végezzük: josamicin, azitromicin. A fenti gyógyszerekkel szembeni egyéni intolerancia esetén a III generációs cefalosporinok alkalmazása elfogadható.
helyi terápia. A chlamydia fertőzésben szenvedő betegek 95% -ánál a mikrobiocenózis különböző súlyosságú diszbiotikus rendellenességei vannak, amelyek a hüvely tartalmának pH-értékének 5,9-re történő emelkedésével járnak. Ezenkívül az urogenitális chlamydiában szenvedő betegek gyakran jelentős szennyeződést szenvednek a nemzetség élesztőgombáival. Candida. Ezek az eredmények az antibiotikumok, eubiotikumok és gombaellenes szerek együttes alkalmazásának szükségességét jelzik. A helyi terápia magában foglalja a hüvely fertőtlenítését, majd az eubiotikumok orális és helyi kijelölését.
Immunmodulátorok és interferon korrektorok. A chlamydia fertőzés jellegzetes vonása az immunrendszer funkcionális aktivitásának megváltozása, a keringő immunkomplexek szintjének eltérései, a sejtes immunitás gátlása, a vér polinukleáris sejtjeinek és makrofágjainak fagocita aktivitásának csökkenése, valamint az immunrendszer gátlása. nem specifikus testvédelmi faktorok aktivitása. A chlamydiával összefüggő immunrendszeri rendellenességek megelőzése érdekében laktoflóra készítményeket írnak fel (bifidobacteria bifidum, szárított laktobacillusok,
floradophilus), amelyek nemcsak a gyomor-bél traktus mikrobiocenózisát korrigálják, hanem a mesenterialis nyirokcsomók csecsemőmirigy-függő zónáit stimulálva aktiválják az immunválaszt. A növényi adaptogének immunmoduláló tulajdonságokkal rendelkeznek, amelyek növelik a szervezet általános nem specifikus ellenállását a fertőzésekkel szemben. A rekombináns interferon gyógyszerét nagy hatékonysággal használják.
A magzati placenta komplex diszfunkcióinak megelőzése. Az uteroplacentáris véráramlás javítására vazoaktív gyógyszereket és thrombocyta-aggregációt gátló szereket használnak. Anyagcsere-terápiaként magas fehérjetartalmú étrendet, erjesztett tejtermékeket írnak elő, enzimkészítmények egyidejű alkalmazásával. A tokoferol-acetátot (E-vitamin), a májvédő szereket metabolizmust aktiváló gyógyszerekként használják.
Szifilisz
A veleszületett szifilisz a placentán keresztüli terjedés következtében alakul ki Treponema pallidum anyától magzatig. Az anya fertőzésének friss formái esetén a magzat fertőzésének kockázata viszonylag magas a betegség késői stádiumában jelentkező fertőzés kockázatához képest. Szinte minden olyan gyermek fertőzött, akinek anyja a terhesség alatt a kezeletlen szifilisz korai szakaszában szenved, és a halálozási arány nagyon magas. Korábban úgy gondolták T. pallidum 18-20 hetes terhesség után kezd átjutni a placentán, amikor a Langerhans-sejtek rétege eltűnik. Mára bebizonyosodott, hogy a magzat transzplacentáris fertőzése korábban is felléphet, de a magzat immunológiai éretlensége miatt a fertőzésre nincs jellemző reakció. Megfelelő festési módszerek alkalmazásával az első trimeszterben az abortusz során kimutathatóak a spirocheták az embriókban.
A fertőzés a korai magzati időszakban halvaszületéssel, macerációval és magzatvízkórral végződik. Általában a vetélésnek jellegzetes megjelenése van: összeesett koponya, kiálló has, hepatosplenomegalia, hólyagos bőrelváltozások, sdfd. Szövettanilag jellemző areaktív nekrózis olyan szervekben, amelyekben a spirocheták fészkek vagy glomerulusok formájában halmozódnak fel a nekrotikus gócok központjában. Proliferatív változások nem jellemzőek. A méhlepényben fokális villusitis uralkodik jellegzetes endarteritisszel a megjelenés típusának megfelelően.
terational angiopathia, valamint a bolyhos fa különféle éretlenségei.
Klinikai megnyilvánulások. A veleszületett szifilisz egy multiszisztémás betegség, amelynek súlyossága és formái nagyon változatosak. A terhesség alatti elsődleges vagy másodlagos kezeletlen szifiliszben szenvedő anyák újszülötteinek 50%-ánál alakul ki (a fennmaradó 50% halva születik, nagyon koraszülött és a korai újszülöttkori időszakban halt meg). Megnyilvánulásai a másodlagos szifiliszhez hasonlítanak.
A veleszületett szifilisz megnyilvánulásai
1. Vetélés vagy halvaszületés: macerált magzat, összeesett koponya, kiálló has, hepatosplenomegalia, hydrops fetalis, hólyagos bőrmegnyilvánulások.
2. Csepp magzat.
3. Kórosan megnagyobbodott placenta (a gyermek lehet normális, nyilvánvalóan fertőzött vagy halva született).
4. Koraszülés.
6. Mucocutan megnyilvánulások: tartós rhinitis, makulopapuláris, hámló vagy bullosus kiütések, általában a tenyéren és a lábfejen.
7. Hepatosplenomegalia, lymphadenopathia.
8. Vérszegénység, thrombocytopenia
9. Sárgaság (hepatitis és/vagy hemolízis).
10. Csont elváltozások: szimmetrikus osteochondritis, periostitis, hosszú csontok, koponya, gerinc és bordák osteomyelitise. Tipikus röntgenkép, pszeudo-bénulás alakulhat ki később.
11. A központi idegrendszer károsodása, általában tünetmentes. A károsodást a cerebrospinális folyadék változásai jelzik.
A legtöbb élveszületés egészségesnek tűnik, néhányuknak hólyagos bullous elváltozások vannak a tenyéren és a talpon, de a következő tünetek jelentkezhetnek a születés után 4 nappal:
1) influenzaszerű szindróma:
meningealis tünetek;
könnyezés (az írisz gyulladása);
Váladék az orrból; a nyálkahártya hiperémiás, ödémás, erodált;
Angina (a garat nyálkahártyáján papulák vannak);
Generalizált ízületi fájdalom (a fájdalom miatt a végtagokban nincsenek aktív mozgások - Parro pszeudoparalízis; a röntgenfelvételen - az osteochondritis jelensége, a periostitis gyakran megfigyelhető, különösen a sípcsont (kardlábak);
2) a nyirokcsomók összes csoportjának növekedése:
Nyaki, könyök, inguinalis, hónalj, popliteális;
Hepatosplenomegalia (súlyos esetekben - vérszegénység, purpura, sárgaság, ödéma, hipoalbuminémia);
3) kiütések:
makulopapuláris;
A papuláris elváltozások összeolvadása széles condylomák kialakulásával.
Megelőzés. A veleszületett szifilisz megelőzése a terhes nők szűrővizsgálatára korlátozódik a betegek időben történő azonosítása érdekében. Amikor a terhesség első trimeszterében diagnosztizálnak, annak megszakítása indokolt, tekintettel arra, hogy a terhesség korai szakaszában bekövetkezett fertőzés súlyos elváltozások kialakulásához vezet a magzatban. Ha a szifiliszt a terhesség késői szakaszában észlelik, a kezelést az Orosz Föderáció Egészségügyi Minisztériumának ajánlásai szerint végzik, az általánosan elfogadott sémák szerint, a betegség lefolyásának stádiumától függően.
Veleszületett szifilisz gyanúja vagy megerősítése esetén az újszülött izolálása szükséges a specifikus terápia megkezdéséig és a kezelés megkezdésétől számított további 24 óráig.
Kezelés. A specifikus terápiát újszülötteknél a következő klinikai helyzetekben végezzük:
Ha az anya kezelése nem volt megfelelő;
Ha a terhesség utolsó 4 hetében végezték;
Ha semmit sem tudni róla;
Ha a penicillintől eltérő gyógyszereket használtak a kezelésre.
Ezenkívül a reagin tesztek eredményeit is figyelembe veszik. Az anyánál magasabb antitesttiter aktív fertőző folyamatot jelez. Az antitesttitert idővel ellenőrizni kell, mivel ez csak az anyai antitestek transzplacentáris átvitelét jelezheti a magzatba. Ha az antitest-titer csökken az élet első 8 hónapjában, akkor az újszülött nem
fertőzött. Pozitív teszteredmény esetén a kezelést azokban a megfigyelésekben kell elvégezni, amikor az antitesttiterek időbeli szabályozása nem lehetséges.
A veleszületett szifilisz kezelésére választott gyógyszer a penicillin G (prokainepenicillin, benzatinepenicillin). A gyógyszer napi adagját az újszülött testtömegétől és életkorától függően számítják ki.
A kezelés hatékonyságának nyomon követése kvantitatív non-treponemális tesztek eredményei alapján történik, amelyeket 3, 6 és 12 hónapos korban végeznek. A negatív teszt eredménye a kezelés hatékonyságát jelzi. Az antitest-titer megőrzése és növelése további vizsgálatot és újbóli kezelést igényel.
Vírusos hepatitisz
Az akut vírusos hepatitist legalább öt különböző kórokozó okozhatja, de az Epstein-Barr vírus, a citomegalovírus és a sárgaláz vírus által okozott májfertőzések külön betegségnek minősülnek, és általában nem szerepelnek az "akut vírusos hepatitis" kifejezésben.
Kioszt:
Vírusos hepatitis A;
Vírusos hepatitis B;
Vírusos hepatitis, sem A, sem B (szórványos és járványos), beleértve a hepatitis C-t (HCV);
Vírusos hepatitis D (egyidejű fertőzés hepatitis B-vel - társfertőzés és szekvenciális hepatitis B fertőzés - felülfertőzés).
A hepatitis A vírus (HAV) a Picornovírusok családjába tartozó enterovírusok nemzetségébe tartozik. Az RNS-tartalmú vírus burok nélküli virionból áll.
A Hepatitis B vírus (HBV) a legtöbbet tanulmányozott. A hepadnovírusokhoz tartozik, szerkezete bonyolultabb, mint a hepatitis A vírusé. A fertőző részecske egy magból (cortex) és egy külső héjból (kapszid) áll. A virion összetétele körkörös kétszálú DNS-t és DNS-polimerázt tartalmaz; A vírusrészecskék replikációja a fertőzött hepatociták sejtmagjában történik.
Legalább négy különböző antigén-antitest rendszer kapcsolódik a hepatitis B vírushoz.
1. A Surface AG (HBsAg, Australian AG) a vírus fehérjeburkához kapcsolódik. A vérplazmában történő kimutatása lehetővé teszi az akut hepatitis B diagnosztizálását, és azt jelenti, hogy a beteg vére potenciális fertőzésforrássá vált. A HBsAg-t az inkubációs periódus alatt (1-6 héttel a betegség klinikai és biokémiai tüneteinek kialakulása előtt) észlelik, és a gyógyulás után eltűnik. Megfelelő antitestek (anti-HB-k) kimutathatók, ami azt jelenti, hogy később, hetekkel vagy hónapokkal a klinikai gyógyulást követően jelenlétük múltbeli fertőzésre és a jövőbeni relatív védettségre utal. 10%-ban a HBsAg továbbra is kimutatható az akut fázis után, és a megfelelő antitestek nem jelennek meg - az ilyen betegek általában krónikus hepatitisben szenvednek, vagy tünetmentes vírushordozókká válnak.
2. A Core AG (HBcAg) a virion magjához (magjához) kapcsolódik. Megtalálható a fertőzött májsejtekben, a plazmában pedig csak akkor mutatható ki, ha a vírusrészecskéket speciális technikákkal elpusztítják. A megfelelő antitesteket (anti-HBc) általában a manifesztációs periódus elején mutatják ki; ezt követően titerük fokozatosan csökken. Az AT-HBc jelenléte az AT-HB-kkel együtt korábbi fertőzésre utal.
3. Az e-antigén (HBeAg) nyilvánvalóan egy peptid, amely a vírusmag része. Csak a HBsAg-pozitív plazmában található. A jelenlét a vírus aktív replikációját jelzi, és a vér fokozott fertőzőképességével és a krónikus májkárosodás kialakulásának valószínűségével párosul.
A hepatitis D vírus (HDV, delta faktor) egyedülálló. RNS-e hibás, aminek következtében ez a vírus csak HBV jelenlétében képes szaporodni. A hepatitis D vagy társfertőzésként fordul elő akut hepatitis B-ben, vagy felülfertőződésként jelentős mértékben krónikus hepatitis B-ben. A fertőzött hepatociták HBsAg-vel bevont delta részecskéket tartalmaznak. Klinikailag a fertőzés az akut hepatitis B szokatlanul súlyos lefolyásával jár.
A non-A non-B hepatitis (NANB) kifejezés olyan fertőzésekre utal, amelyek nem kapcsolódnak A- és B-típusú vírusokhoz. Viszonylag a közelmúltban azonosítottak egy, a flavivírusokhoz hasonló, egyszálú RNS-vírust (hepatitis C vírus), amely
a legtöbb transzfúzió utáni és szórványos NANB-hepatitis esetet okoznak. A HCV jellemzője genomjának rendkívül nagy heterogenitása. A vírusnak legalább hat fő genotípusát azonosították. Az anti-HCV antitestek gyakran megjelennek a plazmában néhány hónappal az akut fertőzés után. A titerek ezután fokozatosan csökkennek, hacsak a fertőzés nem válik krónikussá (ami 50%-ban így van). A HCV vírust a plazmában komplex technikával azonosítják, a megfelelő antigént hepatocitákból izolálják.
Vírus hepatitisz A főként széklet-orális úton terjed, a véren és a kiválasztási termékeken keresztüli fertőzés is lehetséges. A fertőzés forrása csak a betegség korai szakaszában lévő beteg – a vírushordozók és a fertőzés krónikus formái kizártak. A prodromális (preikterikus) stádiumot akut láz, hidegrázás, fejfájás és dyspeptikus zavarok jellemzik. Ebben a szakaszban gyakran megfigyelhető viszketés, amelyet a máj méretének növekedése, a transzferázok szintjének növekedése kísér a vérben 5-7 nappal a sárgaság kialakulása előtt. A fertőzés gyakran tünetmentes.
Vírus hepatitisz Báltalában parenterálisan terjed: fertőzött vérrel és származékaival. Lehetséges fertőzés tetoválás közben. A fertőzés továbbra is magas a kábítószer-függők körében, és megnő a kockázat a hemodializált betegek és a vérrel érintkező kórházi személyzet esetében. Nem parenterális szexuális terjedés van. A krónikus HBV-hordozók a fertőzés tárolójaként szolgálnak.
A HBV fertőzést a májelváltozások széles köre kíséri, a szubklinikai hordozástól az akut és krónikus hepatitisig, cirrhosisig és hepatocellularis karcinómáig. Hosszú lappangási idő (6 hét-6 hónap) után az akut fertőzés jelei jelennek meg. A preikterikus periódus a hepatitis A-val ellentétben hosszabb ideig tart, és fokozatosan fellépő ízületi fájdalmak, csalánkiütések, dyspeptikus és aszténiás zavarok, valamint a hepatolienalis szindróma növekedése jellemzi. A betegség súlyos formáiban a hőmérséklet emelkedik. A vérben - a transzaminázok emelkedett szintje; HBsAg, HBeAg és
A sárgaság megjelenésével a mérgezés, a dyspeptikus, aszténiás megnyilvánulások fokozódnak, és még inkább - a hepatolienális szindróma.
A sárgaság lefolyása kifejezettebb. Súlyos esetekben hemorrhagiás szindróma, akut hepatikus encephalopathia kómába való átmenettel és akár halállal is kialakulhat.
A hepatitis B-ben szenvedő terhes betegeknél magas a koraszülés és a preeclampsia előfordulása. A nők több mint 50%-ának gyulladásos elváltozásai vannak a szülés után.
Hepatitis vagy Ani B(NANB) a hepatitis A-hoz hasonló változattal rendelkezik, amely túlnyomórészt víz útján terjed. A hepatitis B-hez közel álló, általában rövidebb lappangási idővel rendelkező változat gyakran krónikus hepatitis kialakulásához vezet.
Végül a fertőzésnek vannak vegyes változatai (A és B, B és D, B és CMV, B és HIV).
A hepatitis A fertőzés lappangási ideje átlagosan 2-6 hét, hepatitis B - 6-25 hét, sem A, sem B - 2-25 hét. Gyermekek és fiatal felnőttek gyakrabban érintettek, de a betegség bármely életkorban előfordulhat.
A vírusos hepatitis a terhesség alatti sárgaság leggyakoribb oka. Általában viszonylag könnyen lezajlik, de alultápláltság esetén a hepatitis súlyos, járványos formája, sem A, sem B nem fordulhat elő.Az anyai mortalitás 0,64-1,79%, de elérheti a 15,6%-ot (Farber N.A. et al., 1990). A hepatitis súlyosabb a terhesség második felében, ami a hormonszint változásával, a cholestasis kifejezettebb tüneteivel jár.
Veleszületett vírusos hepatitis ritkán fordul elő, az anya akut vagy krónikus hepatitis B-vel a terhesség alatt; Ezenkívül a hepatitis tünetmentes formájával (antigénhordozó) szenvedő anya méhen belüli fertőzés forrása lehet. A magzati hepatitist a hepatocita polimorfizmus jellemzi többmagvú szimplasztsejtek képződésével, valamint kolesztázis (intracelluláris és intratubuláris), adenomatózus struktúrák kialakulása és biliaris nekrózis, a portális traktusok gyenge limfocita infiltrációjával. A súlyos hepatitis az anyában születés előtti magzati halálhoz vezethet. Makroszkóposan a szülés után a membránok sárgás színe, a méhlepény magzati felszíne figyelhető meg, szövettanilag vetéléseknél számos Kashchenko-Hofbauer sejtet rögzítenek a méhlepény bolyhainak stromájában és a bilirubint felvevő membránokban, minimális gyulladásos változások.
Nem állnak rendelkezésre meggyőző adatok a hepatitis teratogén hatásáról a terhesség első trimeszterében. A hepatitis B vírus a születéskor, vagy ritkábban a méhlepényen keresztül továbbítható az újszülöttnek. A terhesség I. és II. trimeszterében az akut hepatitis B ritkán (5%) kerül át a magzatra. A placentán történő átvitelt nem állapították meg véglegesen, és nagy valószínűséggel olyan e-antigén pozitív anyáknál fordul elő, akik krónikus hepatitis B felületes magas vérnyomás (HBsAg) hordozói, vagy akiknél a harmadik trimeszterben hepatitis B fejlődött ki. A harmadik trimeszterben előforduló betegség esetén a magzat fertőzésének valószínűsége 60-70%. A fertőzés leggyakrabban szülés közben következik be az anyától a magzatig terjedő vér mikrotranszfúziója miatt, vagy a gyermeknek a fertőzött anyai váladékkal való érintkezése következtében a szülőcsatornán való áthaladás során. A pozitív HBeAg teszt (amely magas fokú fertőzést tükröz) 80-90%-os esélyt ad a magzatra való átvitelre. Az ilyen anyáktól származó újszülöttek több mint 85%-a krónikus hordozóvá válik. Ha az anya HBeAg-ellenes antitestekkel rendelkezik (jelenlétük a fertőzés megszűnését jelzi), a fertőzés kockázata csak 25%. Lehetséges fertőzés a szülés utáni időszakban (tejjel, nyállal)
A fertőzött újszülöttek gyakran HBV hordozóivá válnak, és szubklinikai májműködési zavaruk van. Ritka az újszülöttkori hepatitis észlelése.
Előrejelzés. A hepatitis A általában 4-8 hét alatt spontán megszűnik – a legtöbb esetben nem igényel különleges kezelést. Az étrend és a fizikai aktivitás korlátozása nem szükséges. A vetélések gyakorisága nem haladja meg a populációban tapasztalhatót. A magzatot gyakorlatilag nem fenyegeti a fertőzés veszélye, és az újszülött nem igényel profilaxist.
Hepatitis B esetén a prognózis kedvezőtlenebb, mint az A esetében. Különösen vérátömlesztés után, amikor a mortalitás elérheti a 10-15%-ot; 5-10%-ban krónikus forma alakul ki. A terhes nők halálozási aránya 3-szor magasabb, mint a nem terhes nőknél. A hepatitis előfordulása újszülötteknél 45-62%.
A terhes nők számára a legnagyobb veszélyt a NANB hepatitis járványos változata jelenti a terhesség II és III trimeszterében. Szövődmények: vetélések, koraszülések, magas anyai mortalitás, újszülöttkori morbiditás és perinatális mortalitás.
Fertőzések megelőzése és kezelése. A személyes higiénia segít megelőzni a hepatitis A-t. Ha egy terhes nő 7-10 napig érintkezik egy beteg személlyel, egy standard γ -globulin 1,5-3,0 ml egyszer intramuszkulárisan. Egy későbbi időpontban a gyógyszer alkalmazása nem praktikus.
A hepatitis B megelőzése érdekében transzfúziós korlátozásokat kell bevezetni, be kell vezetni a HBsAg-vizsgálattal tesztelt vér használatát. Szükséges a donor HCVAg szűrése. A standard immunglobulin védelmet nyújt a klinikai HAV-fertőzés ellen, és azoknak adják, akik otthoni kapcsolatban állnak egy ismert hordozóval.
A HBV elleni védőoltás egészséges recipiensekben antitestek termeléséhez vezet, és 90%-kal csökkenti a hepatitis prevalenciáját. A dializált, májzsugorodásban és más immunrendszeri betegségekben szenvedő betegek rosszabbul reagálnak a vakcinázásra. Az egészséges emberek kis része nem reagál az AT-HB-k képződésével.
A terhes nők HBsAg-hordozási vizsgálatát már a terhesség korai szakaszában el kell végezni.
A hepatitis C esetében a perinatális fertőzés szerepe a fertőzés terjedésében nem teljesen tisztázott. A hepatitis C vírus RNS kimutatása gyermekek vérszérumában a születést követő 1.-5. napon indokolttá teszi azt a feltételezést, hogy ebben a fertőzésben is prenatális fertőzés áll fenn. A hepatitis C kezelése interferonterápián (interferon, interferoninduktorok), valamint vírusellenes szerek alkalmazásán alapul.
Enyhe és közepesen súlyos hepatitis esetén (bármilyen) a terhesség első trimeszterében a terhesség folytatódhat, mivel a szülés idejére a nő egészséges lesz, és a veleszületett rendellenességek valószínűsége gyermekében nem nagyobb, mint egy egészségesnél. Súlyos hepatitisben a gyógyulás után, a fertőzés lefolyásának jellemzőitől és a terhesség időtartamától függően, javasolt megszakítani: legfeljebb 12 hétig - orvosi abortusz, 12 hét után - hipertóniás nátrium-klorid oldat, prosztaglandin F2a intraamnialis beadása ; intramuszkulárisan prosztaglandin bevezetésével a méhnyak előzetes (12 órás) tágítása után közepes méretű moszattal.
A kezelésben a fizikai pihenés, a kiegyensúlyozott ivás, a terhesség idő előtti megszakításának veszélyének kezelése, lehetőség szerint a fiziológiás szülés időpontjának eltolódása, amely a sárgaság közepette nemcsak nem kívánt fizikai megterhelést, hanem hirtelen hormonális megterhelést is hordoz magában. fontosak azok a változások, amelyek kimozdíthatják a szervezetet a kompenzált relatív egyensúlyból. Óvatos infúziós méregtelenítő terápia látható a diurézis irányítása alatt. Folyadékvisszatartás esetén diuretikumokat használnak. A glükokortikoidok rövid kúrája - az agyi ödéma kialakulásában a kiszáradásra vonatkozó intézkedések szerves részeként. A kortikoszteroid terápia kijelölése nem praktikus, és akár a hepatocytodystrophia növekedéséhez is hozzájárulhat.
A HBsAg-pozitív anyától született gyermekeket, függetlenül attól, hogy van-e szérum HBe antigénje vagy antitestjei, születésük után azonnal profilaktikus kezelésben kell részesülniük hepatitis B immunglobulinnal (HBIg), majd háromszor oltást kell kapniuk rekombináns hepatitis vírus C vakcinával. Izolálás anyáktól származó újszülötteknél és a szoptatás megtagadása nem javasolt, különösen a HBIg és a vírusellenes vakcina bevezetése után. Ha a HBsAg az újszülöttkori fertőzés megelőzésére kiválasztódik az anyatejbe, a szoptatás nem javallt.
Az akut hepatitis B-ben szenvedő újszülöttek kezelése megfelelő táplálkozás mellett tüneti; sem a szteroidok, sem a HBIg nem hatékonyak. A fertőzött újszülöttet elkülöníteni kell, és rendkívül óvatosan kell eljárni, amikor vérével és szarjával dolgozik.
TERHESSÉG ELŐKÉSZÍTÉSE ÉS A TERHESSÉG KEZELÉSE
Így az intrauterin fertőzések komoly veszélyt jelentenek a magzat és az újszülött életére és egészségére, és gyakran káros hosszú távú következményekkel járnak. A terhes nők fertőző betegségeinek diagnosztizálása és kezelése jelentős nehézségeket okoz a klinikai megnyilvánulások elmosódása, változatossága és nem specifikussága, a laboratóriumi vizsgálatokhoz szükséges anyag beszerzésének nehézségei, valamint a terápiás gyógyszerek széles körű alkalmazásának lehetetlensége miatt.
A fentiekkel összefüggésben kiemelt jelentőséggel bírnak az anyai fertőzés megelőzésére és kezelésére épülő IUI prevenciós módszerek. Ebben az irányban a legígéretesebb a házaspárok gravidát megelőző felkészítése, majd a terhesség alatti diagnosztikai és kezelési intézkedések következetes végrehajtása.
A Pregravid készítménynek tartalmaznia kell:
Kockázati csoport azonosítása anamnézis adatok és klinikai vizsgálat eredményei alapján, kísérő extragenitalis betegségek azonosítása;
Átfogó vizsgálat az immun-, hormonális, mikrobiológiai állapot vizsgálatával;
Etiotrop antibakteriális vagy vírusellenes terápia;
A genitális traktus mikrocenózisának azonosított megsértésének megfelelő korrekciója, majd az eubiotikumok kijelölése;
Betegségek kezelése immunstimuláló és interferonkorrekciós terápia, valamint fizioterápia alkalmazásával;
metabolikus terápia;
Menstruációs rendellenességek és kapcsolódó endokrin betegségek korrekciója;
A szexuális partner kezelése szexuális úton terjedő betegségek jelenlétében.
Terhesség alatt 12 hétig, valamint 18-20, 28-30 és 37-38 hétig az ebbe a csoportba tartozó terhes nőknél a hüvelyi mikrocenózis állapotának felmérése látható, legfeljebb 12 hétig (továbbiakban indikációk 18-20 és 37-38 héten) - a szexuális úton terjedő betegségek kórokozóinak azonosítása, valamint a specifikus Ig titerének meghatározása vírusos és bakteriális ágensekkel szemben. A fertőzések észlelésekor megfelelő kezelést végeznek, amelyet a terhesség időtartamának és a gyógyszerek magzat fejlődésére gyakorolt lehetséges hatásának figyelembevételével választanak ki.
A rendszeres echográfiás, dopplerometriai és kardiotokográfiás vizsgálat lehetővé teszi a kialakuló magzati placenta elégtelenség időben történő diagnosztizálását, kezelését és hatékonyságának nyomon követését.
A gravidáció előtti előkészítés és intézkedések a veszélyeztetett méhen belüli fertőzések azonosítására
lehetővé teszi az intrauterin fertőzések gyakoriságának 2,4-szeres csökkentését. Ezzel párhuzamosan csökken a terhesség és a szülés szövődményeinek száma (különösen a terhesség idő előtti megszakítása, valamint a magzati placenta elégtelensége), ami segít az újszülöttek általános előfordulási gyakoriságának másfélszeres csökkentésében.
Az intrauterin fertőzés különböző megnyilvánulásokkal járhat, attól függően, hogy mennyi ideig történt a magzat fertőzése.
- 3-12. terhességi hét: terhesség megszakadása (spontán vetélés), vagy magzati fejlődési rendellenességek kialakulása (a test normál felépítésétől való eltérések, amelyek méhen belüli vagy ritkábban a szülés utáni fejlődés során jelentkeznek);
- 11-28. terhességi hét: méhen belüli növekedési retardáció lép fel, a baba alacsony testsúllyal születik, magzati fejlődési rendellenességek (pl. szívfejlődési rendellenességek (nem megfelelő válaszfalak kialakítása stb.)).
- 10-40 hetes terhesség: fetopathia (a magzat betegségei; a magzat szerveinek károsodása, például magzati tüdőgyulladás (tüdőgyulladás a magzatban) képződik).
Ha nem volt spontán abortusz (spontán vetélés), és a gyermek a születés előtti időszakban fertőzéssel született, az ilyen gyermekeknél (különböző súlyosságban és különböző kombinációkban) a következő tünetek jelentkeznek:
- intrauterin növekedési retardáció;
- hepatosplenomegalia (a máj és a lép megnagyobbodása);
- korai sárgaság;
- eltérő jellegű kiütések;
- légzésfunkciós zavarok;
- szív- és érrendszeri elégtelenség;
- Neurológiai rendellenességek;
- magas testhőmérséklet az élet első napján;
- gyulladásos (pl. kötőhártya-gyulladás) és degeneratív (pl. látóideg atrófia) szembetegségek.
Az ilyen gyermekek rendellenességek jelei nélkül születnek, de egy idő után (legkésőbb az élet harmadik napján) megjelennek:
- letargia;
- sápadtság;
- étvágytalanság;
- fokozott regurgitáció;
- légzési elégtelenség;
- bármely szerv károsodása (szülés közbeni fertőzés esetén a gyulladást gyakrabban észlelik, mint egy szervet, például tüdőt, májat stb.).
Okoz
- A magzat fertőzése beteg anyától származik.
- Fertőzési mechanizmusok:
- transzplacentális (hematogén) út - az anyától származó kórokozó a méhlepényen keresztül jut be a magzatba (a vírusok és a toxoplazma gyakran ilyen módon terjed);
- felszálló út - a fertőzés útja, amelyben a nemi traktusból származó fertőzés a méh üregébe jut, majd megfertőzheti a magzatot (tipikus a chlamydia fertőzésre, enterococcusokra);
- leszálló út - a petevezetékekből származó kórokozó a méh üregébe, majd a magzat testébe kerül;
- kontakt (intranatális) út - a magzat fertőzése a születési csatornán való áthaladás során következik be, például fertőzött magzatvíz lenyelésekor, amikor a fertőzött magzatvízből származó kórokozó bejut a nyálkahártyákba és a szembe.
- A magzat méhen belüli fertőzésének kialakulásához hozzájáruló tényezők:
- az anya urogenitális rendszerének betegségei (nyaki erózió, fertőzés urethritis (húgycsőgyulladás), cystitis (hólyaggyulladás), pyelonephritis (gyulladásos vesebetegség) stb. formájában;
- terhesség alatt átvitt fertőzések, még SARS (akut légúti vírusfertőzés);
- immunhiányos állapotok, beleértve a HIV-fertőzést;
- szervek és szövetek átültetése utáni állapotok.
Diagnosztika
- A terhesség alatti méhen belüli fertőzés diagnosztizálása nehéz, mivel a magzat méhen belüli fertőzését az anyában nem kísérik specifikus megnyilvánulások.
- A terhesség tervezésének szakaszában a szexuális úton terjedő betegségeket és a leggyakoribb urogenitális fertőzéseket PCR-rel (polimeráz láncreakció) diagnosztizálják. Terhesség alatt diagnosztikát is végeznek ezen betegségek jelenlétére, mivel a terhes nők immunitása fiziológiailag csökken, illetve nő a különböző fertőző betegségekre való hajlam.
- Terhes nő vérének diagnosztizálása TORCH-fertőzés, HIV, szifilisz (bőrt, nyálkahártyákat, belső szerveket, csontokat, idegrendszert érintő nemi betegség), hepatitis B- és C-fertőzés vérének vizsgálatával ellenanyagok (védőtestek) jelenlétére. ezeknek a fertőzéseknek a kórokozói.
- Az M és G védőtestek (immunglobulinok) összetétele és mennyisége is felhasználható a magzat méhen belüli fertőzésének kockázatának megítélésére:
- a specifikus IgG kis mennyiségben történő kimutatása azt jelzi, hogy a fertőzés a múltban volt, immunitás alakult ki ezzel a kórokozóval szemben, és a betegség nem jelent veszélyt sem az anyára, sem a gyermekre;
- az IgG tartalom növekedése vagy az IgM megjelenése a fertőzés kiújulását jelzi. Az intrauterin fertőzés valószínűsége viszonylag alacsony;
- a fertőzés magasságában csak az IgM kimutatható olyan nőnél, aki korábban nem szenvedett egyik vagy másik betegségben. Egyes fertőzések (például herpeszvírus-fertőzés vagy citomegalovírus) esetén a magzat fertőzésének kockázata a terhes nők kezdeti fertőzése során az esetek körülbelül fele.
- Ultrahang vizsgálat a méhlepény működésének, magzati véráramlás diagnosztizálására (a méhlepény szerkezetében bekövetkező változások, pl. megvastagodása, megnövekedett vagy csökkent magzatvíz tartalma, szuszpenzió jelenléte a magzatvízben méhen belüli véráramlásra utalhat a magzat fertőzése).
- Egyes esetekben chorionbiopsziát írnak elő (az embrió külső héjának egy részének begyűjtése a vizsgálat elvégzése céljából), majd magzatvíz-mintavételt, kordocentézist (a magzat köldökzsinórvérének vizsgálata) követik. bakteriológiai vizsgálattal (táptalajra vetés a kifejlett telepek további felmérésével) kórokozó jelenlétére.
- A méhlepény (placenta, membránok és köldökzsinór) vizsgálata bakteriológiai és immunhisztokémiai módszerekkel (a szövetek mikroszkópos vizsgálatának módszere egy adott kórokozó jelenlétére).
- Újszülött vérének szerológiai vizsgálata enzim immunoassay-vel (ELISA) az IgM, IgG, IgA antitestek meghatározására (a gyermek vérében az IgG anyai antitestek bejutását jelezheti, így az újszülött vérét 3. 4 hét; az IgG-tartalom 4-szeres vagy nagyobb növekedése lehetséges fertőző folyamatot jelez.Az újszülött vérében az IgM aktív fertőzés jelenlétét jelzi a gyermekben).
- A méhen belüli fertőzés gyanúja esetén a hasüreg ultrahangját írják elő a megnagyobbodott máj és lép kimutatására, neurosonográfiát (a központi idegrendszer struktúráinak állapotának felmérésére szolgáló módszer).
- Konzultációra is van lehetőség.
Az intrauterin fertőzés kezelése
A kezelés a kórokozótól függ. Kinevez:
- antibakteriális gyógyszerek;
- vírusellenes gyógyszerek;
- immunstimuláló gyógyszerek;
- erősítő szerek;
- tüneti (a tünetektől és az érintett szervektől függően) gyógyszerek.
Komplikációk és következmények
- A terhesség spontán megszakadása (spontán vetélés).
- A magzat veleszületett fejlődési rendellenességei (különösen, ha a magzat fertőzése a fejlődés első 2 hónapjában következik be).
- Az újszülött korai halála (életének első 1-7 napjában).
- Halvaszületés.
- Hosszú távú következmények (például bármely szerv fejlődési rendellenességei, agyciszták stb.).
- veleszületett immunhiány kialakulása.
- A méhen belüli fertőzésben szenvedő gyermekek később szerzett egyéb fertőzéseit súlyos lefolyás, különböző szervek és rendszerek súlyos károsodása jellemzi. Lehetséges:
- fertőző folyamat újszülöttben (ha a magzat fertőzésével való érintkezés röviddel a szülés előtt történt, akkor a gyermek tüdőgyulladással (tüdőgyulladás), enterocolitissel (vékony- és vastagbélgyulladás), agyhártyagyulladással (agyhártya-gyulladás) születhet stb.);
- fertőző ágens hordozásának kialakulása a betegség jövőbeni kialakulásának kockázatával. A bakteriohordozó olyan állapot, amikor a szervezetben kórokozó van, de a betegségnek nincsenek klinikai tünetei;
- ha a gyermek jóval születése előtt megbetegszik, akkor egészségesen, de kis testsúllyal (2500 gramm alatt) születhet.
Az intrauterin fertőzés megelőzése
A terhesség tervezési szakaszában és a terhesség alatt:
- a várandós anya diagnózisa szexuális úton terjedő betegségek jelenlétére;
- vérvizsgálat a TORCH-komplex fertőző ágensek elleni antitestek (védőtestek) jelenlétére (például ha a vizsgálat során kiderül, hogy a nőnek nem volt rubeola, akkor a terhesség tervezésekor (legalább 6 hónappal korábban) , oltás szükséges), HIV, szifilisz (bőrt, nyálkahártyákat, belső szerveket, csontokat, idegrendszert érintő nemi betegség) és hepatitis B és C;
- kerülje a beteg rokonokkal való érintkezést;
- megvizsgálja a háziállatokat (például a macskákat toxoplazmózis jelenlétére);
- ne egyen gyorséttermeket, félkész termékeket, csak jól sült húst és halat egyen, hagyja fel az egzotikus konyhát;
- rendszeres látogatás a terhesség alatt (1. trimeszterben havonta 1, 2. trimeszterben 2-3 hetente 1, 3. trimeszterben 7-10 naponként 1 alkalommal);
- egy terhes nő időben történő regisztrációja a terhességi klinikán (legfeljebb 12 hetes terhesség);
- a terhességre való időben történő felkészülés és annak tervezése (időben történő védőoltás, például rubeola ellen, az urogenitális rendszer betegségeinek kimutatása és kezelése stb.);
- a női reproduktív rendszer fertőző és gyulladásos betegségeinek időben történő és megfelelő kezelése.
Továbbá
- A legveszélyesebb kórokozók, amelyek szinte mindig súlyos magzati patológia kialakulását okozzák, az úgynevezett TORCH komplexben kombinált fertőzések:
- Hogy (Toxoplasma gondii) - toxoplazmózis;
- R (Rubella vírus) - rubeola;
- C (CMV) - citomegalovírus;
- H (Herpesz vírus) - herpesz.
- A szexuális úton terjedő betegségek (chlamydia, mycoplasma fertőzések, trichomoniasis, gonorrhoea) szintén okozhatnak magzati patológiákat.
- A szifilisz a magzatra is különösen veszélyes.