Kaj so intrauterine okužbe? Okvare urinarnega sistema. Intrauterina okužba - norice.
Tradicionalno v ruski literaturi pod izrazom "intrauterine okužbe"(IUI) se nanaša na bolezni, pri katerih se okužba pojavi v prenatalnem obdobju ali med porodom, vir pa je mati. Treba je opozoriti, da se intrauterina okužba otroka od matere pojavlja veliko pogosteje, kot se razvije. Klinični znaki bolezni. Za navedbo dejstva intrauterine okužbe v praktična medicina uporabite izraz "intrauterina okužba". Termin "intrauterina okužba" se običajno uporablja za sklicevanje na klinične manifestacije nalezljiva bolezen ploda in novorojenčka, odkrita prenatalno ali kmalu po rojstvu.
Intrauterina okužba - rdečke
Rentgenski žarki pljuč kažejo mikrobe in mrežaste sence, debel utrip, nejasen srčni utrip. Paraklinične študije: hemogram - levkocitoza z zvišano telesno temperaturo, limfomonocitoza, trombocitopenija; kritično nizke skupne beljakovine in albumin. Diagnoza neonatalna sepsa pri več organih, sindrom respiratorne stiske, hud meningoencefalitis, možganska krvavitev. Na četrti rojstni dan se otrok usodno konča. Med porodom ima otrok težave pri prilagajanju.
Pogostost intrauterine okužbe. Po posplošenih literaturnih podatkih je najmanj 10 % novorojenčkov v maternici okuženih z različnimi virusi in mikroorganizmi. Tveganje za intrauterino okužbo je odvisno od vrste patogena, začetnega zdravstvenega stanja nosečnice in ploda ter epidemiološke situacije v določeni geografski regiji. Večjo pogostnost opazimo pri primarni okužbi nosečnice kot pri latentni ali sekundarni virusni okužbi.
Z intenzivnim intenzivna nega beležijo se progresivno poslabšanje, povečana zlatenica, zvišana telesna temperatura in vročinski izločki iz oči. Novorojenčka intubiramo pri 30 urah in začnemo z ventilacijo. Hkrati se je pojavil petehialni izpuščaj, generaliziran edem, klonično trzanje spodnjih okončin, krvavitev iz dihalnih poti. Četrti dan po rojstvu so LM izolirali iz hemokulture, tekočine, oči, ušesa in sapnik. Otrok se posvetuje nalezljiva oseba etiološko zdravljenje se spremeni, surfaktant se aplicira dvakrat, vendar pljučna funkcija ostane nespremenjena.
Intrauterine okužbe so pomemben razlog reproduktivne izgube. Tako se pogostost zgodnje neonatalne obolevnosti in umrljivosti pri IUI giblje od 5,3 do 27,4 %, stopnja mrtvorojenosti pa doseže 16,8 %. V strukturi perinatalne umrljivosti predstavlja okužba 10,1 %. Še pomembnejša vloga nalezljivih vnetne bolezni igrajo v strukturi perinatalne obolevnosti, kjer predstavljajo 20-38%.
Zdravljenje in spremljanje intrauterine okužbe
Kljub ustrezni antibakterijski in imunomodulatorni terapiji ostane otrok do 12. dne po rojstvu odvisen od prezračevanja prostora. Obdobje okrevanja je počasno, otrok ima zmanjšan mišični tonus, sesalni refleks, tahidispneja, obilno izločanje zgornjih dihal in stalno pljučno zaznavanje majhnega vlažnega žvižgajočega krizma. 30. dan je bila napisana na željo sorodnikov, nato pa postavljena v posebno hišo zdravstvena oskrba. Zdravljenje: uporabno prezračevanje; površinsko aktivna snov - dvakrat; antibiotiki - cefuroksim, amikacin, meropenem, fortum, ampicilin, linezolid, intravenske infuzije in vitamini, flukonazol, humani albumin, 3-mesečni imunovenin, transfuzijo plazme in transfuzijo krvi.
Hkrati ostaja resnična pogostost perinatalne patologije, ki jo povzroča infekcijski dejavnik, še vedno nedorečena, kar je posledica pomanjkanja presejalnih študij, neskladja med pogostostjo okužbe in neposredno obolevnostjo ter pogostega latentnega poteka. patološki proces, objektivna kompleksnost predporodne laboratorijska diagnostika. Kot rezultat
Otrok je vzgojen v domu socialnega varstva; Odstopanja v nevropsihičnem razvoju so resna, hidrocefalus vztraja in se poglablja. Listerioza je akutna nalezljiva bolezen, pri kateri se razvije septikemija. klinična slika s poškodbo več organov s prednostno prizadetostjo centralnega živčnega sistema pri starejših, pri nosečnicah pa presajenih huda škoda plod, ki vodi do splava ali možganske kapi.
Zgodnja identifikacija etiološkega povzročitelja in ustrezna antibiotična terapija upodobljeno ugoden vpliv za listerijske okužbe. Septično stanje in odstopanja parakliničnih parametrov se hitro odpravijo, vendar škodljivi učinki na plod zahtevajo prekinitev nosečnosti po medicinske indikacije. Opisane motnje pri novorojenčkih ustrezajo literaturnim podatkim. To opozarja zdravnike, da je treba ob prisotnosti tako imenovanega "sindroma gripe" pri nosečnicah obravnavati tudi listeriozo.
Tako velik del okužb ostaja neprepoznan in se v statistični analizi upošteva kot posledica zapletov porodnega akta, intrauterine asfiksije, sindroma respiratorne stiske in drugih patoloških stanj.
V 95,8 % so vzrok smrti zaradi infekcijskega procesa stanja, ki se pojavijo v perinatalnem obdobju. Od teh so najpogosteje opaženi: prirojena pljučnica 47,5 %, okužbe, specifične za perinatalno obdobje 41,6 %, in neonatalna sepsa 6,7 %.
Preprečevanje okužbe ploda
Etiološka prefinjenost in ustrezna antibiotična terapija bosta zaščitila plod pred resnimi poligonalnimi poškodbami. Načela in praksa nalezljive bolezni. Nalezljive bolezni in nosečnosti. Nalezljive bolezni matere in intrauterinega ploda. Vse več primerov listerioze v Franciji in drugih evropskih državah. Izbruh neonatalne listerioze, povezane z mineralnim oljem.
Monocitogena okužba z listerijo med nosečnostjo - sodobnih vidikov. Listerioza med nosečnostjo: poročilo o primeru. Klinična predstavitev in izid v primerih listerioze. Zaradi tega je preprečevanje prenosa z matere na otroka ena izmed pomembne komponente perinatalna oskrba. Zato je eden najpomembnejših ciljev perinatalne oskrbe preprečiti prenos okužbe z matere na novorojenčka.
Etiologija. Seznam brezpogojnih patogenov je precej obsežen in vključuje na desetine vrst skoraj vseh razredov organizmov od virusov do protozojev in gliv.
Odstotek otrok, rojenih s simptomi bakterijski intrauterinih okužb je 20-36%. Trenutno je dokazana vloga širokega spektra aerobnih in anaerobnih bakterijskih sredstev, predvsem predstavnikov oportunistične mikroflore: stafilokokov, streptokokov, coli, Klebsiella, Proteus, Enterobacteria, pa tudi anaerobni mikroorganizmi, ki ne tvorijo spor. Opozoriti je treba, da se pri tej skupini bolnikov običajno odkrijejo pomembne motnje v sestavi vaginalne mikrobiocenoze (60-65% ima vulvovaginalno kandidozo ali bakterijsko vaginozo).
Bistvo sepse je vnetni odziv telesa na infekcijski dražljaj, povezan s pojavom bakterij v krvi. Večino jih ogrozi dojenček, kar lahko privede do odpovedi organa. Eden najpomembnejših klinične raziskave je anamneza, v kateri je treba oceniti potek nosečnosti in poroda. Zgodnja neonatalna sepsa se najpogosteje pojavi med dnevom življenja, izjema pa je celo nekaj ur po rojstvu. Pozna neonatalna sepsa se pojavi med dnevi življenja.
Zapleti neonatalne sepse
Drugi zapleti neonatalne sepse vključujejo dihalne, srčno-žilne, presnovne zaplete, osteomielitis in druge.
Preventivni in profilaktični ukrepi za preprečevanje okužbe
Zdravljenje novorojenčka med sepso. Novorojenčka s septično okužbo premestijo v posredniško enoto, kjer ga spremlja in zdravi zdravstveno osebje. Še posebej je pomembna skrbna manipulacija, ki olajša zaznavanje bolečine pri tej bolezni. Takoj, ko se zdravje novorojenčka izboljša, se vrne v materino sobo.Klasičen primer bakterijske IUI je listerioza, ki jo povzroča Listeria monocytogenes- kratke gram-pozitivne paličice (kokobacili). Med drugimi bakterijskimi povzročitelji intrauterine okužbe se je v zadnjih letih povečala vloga streptokokov skupine B. Njihov pomen v patologiji ploda, zlasti pri novorojenčkih, se je v ozadju obsežnega uvajanja aminoglikozidnih antibiotikov v prakso, ki jim ti mikroorganizmi močno povečajo. so naravno odporni. Trenutno je bila ugotovljena tesna povezava med pogostostjo okužb, ki jih povzročajo streptokoki skupine B pri novorojenčkih, in pogostostjo prenašanja teh bakterij v genitalnem traktu mater. Pogostost odkrivanja streptokokov skupine B pri nosečnicah se zelo razlikuje - od 1,5 do 30%. Najbolj nevarno je masivno žarišče (več kot 10 5 CFU / ml) v materničnem kanalu materničnega vratu. V takih primerih se več kot 60 % novorojenčkov rodi okuženih. Klinične manifestacije okužb, ki jih te bakterije povzročajo pri novorojenčkih, so raznolike – od lokalne kože
Ženske so med nosečnostjo izpostavljene širokemu spektru patogenov. Razvoj okužbe je tako pogost kot nosečnost. Izjema je povečano tveganje okužba ploda. Nekateri patogeni imajo povečano afiniteto do placentnih trofoblastov, kar povzroča vnetje, ki mu sledi okužba ploda. Okužba se lahko pojavi prenatalno, perinatalno ali v neonatalnem obdobju. Prenos povzročitelja okužbe z matere na plod se imenuje navpičen.
Prenatalne okužbe delimo na embriopatije in fetopatije, odvisno od obdobja nosečnosti, v katerem se motnja pojavi. Embriopatije se pojavijo v prvem trimesečju nosečnosti in zanje so značilne teratogene malformacije. Med blastogenezo povzročitelj vstopi v zarodek in običajno umre. V fazi organogeneze se materino sredstvo prenaša na plod po hematogeni poti, vendar posteljica, vključno s fetoplacentno cirkulacijo, ni v celoti razvita, kar omejuje prenos sredstva na plod.
do hudih fulminantnih septičnih procesov in meningitisa, ki jih spremlja visoka smrtnost (do 80%) pri nedonošenčkih.
V zadnjih letih je v strukturi perinatalne patologije pomemben pomen ssualno-prenosno intracelularno povzročitelji infekcij: mikoplazme, ureaplazme in klamidija. Pogostnost intrauterine okužbe z genitalno sečnino in mikoplazmozo pri nosečnici je 40-50%, pri klamidiji pa 70,8%.
Fetopatija nastane iz meseca nosečnosti in ni anatomskih nepravilnosti, funkcija prizadetih organov je običajno okvarjena. Prenos poteka po hematogeni poti ter tik pred in po rojstvu. Intracelularni patogen vstopi v fetoplacentno cirkulacijo. Teratogeneza ploda ima večfaktorske vzroke, vključno z genetiko, zdravili in izpostavljenostjo okolja.
Posledica okužbe med nosečnostjo je lahko. Rojstvo novorojenčka z nizko porodno težo zaradi intrauterine zaostalosti rasti ali prezgodnjega poroda. Teratogena malformacija – najbolje dokumentiran teratogen je virus rdečk. Aktivne prirojene okužbe - pojavijo se pred rojstvom, povzročitelj okužbe pa je prisoten tudi po rojstvu. Splav, prezgodnji porod ali smrt novorojenčka. . Prenatalna okužba Kronični kongenitalni sindrom je opredeljen kot vsaj en mesec okužbe, katere simptomi so bili očitni že ob rojstvu.
Precejšen delež perinatalnih okužb povzročajo različni virusi, med katerimi so najpomembnejši citomegalovirusi, herpes simplex, rdečke, enterovirusi (ECHO, Coxsackie), hepatitis B, virus humane imunske pomanjkljivosti. Poleg tega gripa, ošpice, poliomielitis, papiloma in parvovirusi vplivajo na povečanje reproduktivnih izgub in obolevnosti pri novorojenčkih.
Kronični prirojeni sindrom se lahko pojavi kot aktivna okužba z znaki aktivnega vnetnega odziva ali znaki celjenja. Druge kronične prirojene okužbe lahko kažejo simptome prirojene anomalije ali znaki prizadetosti organa kot posledica okužbe.
Perinatalni streptokokne okužbe. Okužba je bila v preteklosti povezana le z kirurški posegi in porod. Glavni etiološki povzročitelji perinatalnih okužb so bili streptokoki. Ta dejstva vzbujajo zaskrbljenost glede tveganja za hudo poporodno okužbo pri novorojenčkih.
V zadnjih letih se povečuje število bolnikov z lokalnimi oblikami herpetičnih lezij, kar določa trend povečevanja pogostnosti okužb s herpesom pri novorojenčkih. Poraz virusa genitalij se odkrije pri 7% nosečnic. Herpes je primer klasične kronične okužbe z doživljenjskim obstojem patogena v gostiteljskem organizmu. Izoliranih je približno 70 vrst virusov te skupine, od tega 4 prizadenejo ljudi: serotipa virusa herpes simplex I in II, virus varicella-zoster, virus Epstein-Barr in citomegalovirus (vsi trije izolirani sevi - Devis, Kerr in AD189). klinični pomen.
Ta priporočila je razvila delovna skupina, odobrila pa sta jih Poljsko ginekološko združenje in Poljsko društvo novorojenčkov. Bolnišnične okužbe so bile v preteklosti le ob kirurških posegih in porodih. Glavni etiološki dejavniki to okužbo so bili streptokoki.
Toksoplazmoza: značilnosti okužbe
To vzbuja veliko zaskrbljenost glede tveganja resnih perinatalnih okužb pri novorojenčkih. Takšne smernice je pripravila delovna skupina, odobrila pa sta jih Poljsko ginekološko društvo in Poljsko društvo novorojenčkov. Neonatalno obdobje je čas, ko se otrokovo telo po prehodu iz intrauterinega v nekonfliktno življenje prilagaja novim razmeram. Po statističnih podatkih pokriva prvih 28 dni življenja.
Precej pogosti v populaciji so enterovirusne okužbe. Kot povzročitelji intrauterinih okužb so najbolj zanimivi ehovirusi in virusi Coxsackie. Poskus je dokazal etiološki pomen virusov Coxsackie tipov A 13, A 3, A 6, A 7, B 4 in B 3 ter ehovirusov 9 in 11 tipov.
Retrovirusi, ki povzročajo AIDS, si zaslužijo posebno pozornost. Do 50 % otrok, rojenih materam, okuženim s HIV, se okuži pred porodom, med porodom ali v zgodnjem neonatalnem obdobju. Incidenca bolezni pri novorojenčkih pri seropozitivnih materah se zelo razlikuje - od 7,9 do 40%.
Občutljivost novorojenčkov za okužbe je posledica nezrelosti imunski sistem, zlasti pri tistih, pri katerih se pogosto uporabljajo invazivni diagnostični in terapevtski postopki. Izraz okužba je razdeljen na. Zelo zgodnje okužbe. zgodnje okužbe.
Osnovna načela zdravljenja okužb
okužbe pozen začetek. Na materini strani - pretok krvi, adenom, kolaps, perinatalna okužba. Perinatalne okužbe so okužbe, ki nastanejo med porodom kot posledica stika novorojenčkovih sluznic z mikroorganizmi, ki so prisotni v materinem genitalnem traktu, zato je glavni vzrok perinatalne okužbe flora maternice, redkeje okolje, predvsem bolnišnica.
Najvišja vrednost med glivične patogeni IUI imajo razširjene predstavnike gliv iz rodu Candida. Kriptokokoza, kokcioidoza, aspergiloza in histoplazmoza pri nosečnicah
nyh se pogosto pojavljajo v ozadju imunske pomanjkljivosti. Opozoriti je treba na dejstvo, da se pogostost kliničnih manifestacij vaginalne kandidiaze med nosečnostjo močno poveča, kar III trimesečje doseže 31-33%. Ta pojav je povezan s kršitvijo absorpcije glikogena v celicah vaginalnega epitelija, pa tudi s povečanjem tvorbe mucina, ki zaradi učinka "razredčitve" vnaprej določi zmanjšanje koncentracije aktivne snovi. dejavniki lokalne imunosti v vaginalnem mediju - lizocim, kationski proteini, sretorna protitelesa itd. hranila v obliki glikogena v kombinaciji z oslabitvijo lokalne imunosti ustvarjajo ugodne pogoje za izvajanje patogenega učinka glivične flore. Glede na DNK diagnostiko se med vaginalnim porodom kontaminacija novorojenčkov pri materah bolnikov s kandidozo približa 100 %, do konca neonatalnega obdobja pa opazimo spontano izločanje gliv le v 35 %, kar kaže na nastanek kandidiaze v ostalo. Pogostnost klinično izražene kandidiaze pri novorojenčkih v prvih 35 dneh se približa 20-30%, kljub zdravljenju pa se po 1 mesecu opazi pri vsakem petem opazovanju. glivična okužba ne povzroča le ustne, genitalne in kožne manifestacije kandidiaza pri novorojenčkih, lahko pa vodi tudi do intrauterine okužbe ploda s tvorbo sistemske mikoze z globoko poškodbo pljuč, možganov, pa tudi do spontanega splava (pogosteje v II trimesečju, v 14-25 tednih).
Okužba s citomegalovirusom pri novorojenčkih
Bolečina in njeno notranje okolje, dokler se ciste ne zlomijo. Po drugi strani pa je na materini poti veliko mikroorganizmov, ki lahko povzročijo okužbo pri novorojenčku. Običajno se nahajajo na površini zdravih odraslih, vendar imajo pod določenimi pogoji sposobnost, da prodrejo v gostiteljska tkiva, se izognejo imunskim odzivom in okužijo. Glavni klinične oblike od teh okužb sta nekrotizirajoči fasciitis in sindrom toksičnega šoka. Kot komenzal lahko ta bakterija zasede nižje prebavila, anus, ženska vagina.
Končno se pojavijo perinatalne okužbe protozoje, treponeme in rikecije. V tej skupini najpomembnejši toksoplazmoza, pogostnost intrauterine okužbe pri kateri je približno 40%. Poleg tega je v zadnjih letih opaziti trend povečanja pogostnosti sifilisa. Prirojeni sifilis se pojavi pri več kot 50 % novorojenčkov od bolnih mater, ki niso prejele ustreznega zdravljenja.
To olajšajo visoke frekvence spolnih razmerij. Glavni povzročitelji bolezni so polisaharid, drugi hemolizin in nevraminidaza. Prisotnost protiteles proti policističnim antigenom v materinem serumu ščiti otroka pred okužbo. Odziv na okužbo je specifičen za antigen. Pri dojenčkih se okužba najpogosteje pojavi med porodom, redkeje kot posledica prezgodnje cistične fibroze.
Vnetje kosti zarodka. Prezgodnji kašelj. Okužba je lahko asimptomatski nosilec, zgodnja okužba – največkrat se pri novorojenčkih kaže sepsa – meningitis in nalezljiva bolezen. Zgodnja okužba, ki se kaže s hitro naraščajočo odpovedjo dihanja, slabim nevrološkim statusom, prehranskimi nepravilnostmi in umrljivostjo, se giblje od 5 do 20 %. Smrtnost zaradi takšnih okužb je 2-6%.
Pomembno je omeniti, da je v večini primerov intrauterina okužba posledica povezave več patogenov ali pa je mešana (virusno-bakterijska, bakterijsko-glivična). V strukturi antenatalne umrljivosti zaradi intrauterine okužbe je 27,2 % virusna infekcija, 26,3% - za mešano in 17,5% - za bakterijsko.
Leta 1971 je bila ugotovljena skupina okužb, ki imajo kljub izrazitim razlikam v strukturi in bioloških lastnostih patogenov podobne klinične manifestacije in povzročajo trajne strukturne okvare ploda različnih vrst. organskih sistemov, med katerimi so najpomembnejše lezije centralnega živčnega sistema. Da to označim nalezljiva skupina A.J. Nahmias (1971) je predlagal okrajšavo BAKLA. Ta kompleks združuje naslednje intrauterine okužbe: T- toksoplazmoza, R- rdečke (rdečke), C- okužba s citomegalovirusom, H- okužba s herpesvirusom.
V zadnjih 15 letih je prišlo do spremembe etiološke strukture perinatalnih okužb. To je deloma posledica povečanih možnosti specifična diagnoza, predvsem mikoplazmoza, klamidija, citomegalija, herpetična in okužba s streptokokom B in drugi. Obstaja tudi resnična sprememba patogenov, zlasti listerije (Ailama-
Zyan E.K., 1995).
Kljub širok spekter patogenov, je treba opozoriti, da imajo vse intrauterine okužbe skupne značilnosti:
Latentni ali izbrisani potek, ki znatno otežuje diagnozo (zlasti z intracelularno lokalizacijo patogena - klamidija, mikoplazme, virusi itd.) in ne omogoča pravočasnega začetka etiotropne terapije;
Aktivacija latentno obstojne okužbe je možna s kakršno koli kršitvijo homeostaze pri nosečnici (anemija, hipovitaminoza, prekomerno delo, stresne situacije, dekompenzacija ekstragenitalne bolezni neinfekcijske narave).
POTI INTRAUTERINE INFEKCIJE IN MEHANIZEM OKUŽBE PLODKA
Intrauterina okužba se pojavi na naslednje načine: "vzpenjajoče se- ob prisotnosti specifične lezije spodnjega dela
odseki genitalnega trakta (slika 34); "hematogeno(transplacentalno) - v večini primerov zaradi sposobnosti nekaterih mikroorganizmov, da dolgo vztrajajo v limfocitih periferne krvi;
transdecidualno(transmuralno) - v prisotnosti okužbe v endometriju;
riž. 34. Patogeneza naraščajoče intrauterine okužbe
padajoče- z lokalizacijo vnetnega žarišča na območju materničnih dodatkov;
*nalezljiv- neposredna kontaminacija novorojenčka pri prehodu skozi porodni kanal;
mešano.
Bakterijska intrauterina okužba z oportunističnimi patogeni se razvije predvsem zaradi naraščajoča okužba iz porodnega kanala. Ta pot je značilna tudi za mikoplazme, klamidijo, glive iz rodu Candida in le nekateri virusi, zlasti herpes simplex. Predisponirajoči dejavniki so urogenitalne okužbe, istmiko-cervikalna insuficienca, delna ruptura membran, nepravočasen odtok vode, biopsija horiona, amniocenteza.
Ascendentna okužba se najhitreje pojavi, ko so membrane poškodovane. Amnijska tekočina ženske pozne zmenke nosečnost ima protimikrobno delovanje, ki pa je šibko izraženo in lahko le odloži (vendar
ne zavirajo) rasti mikroorganizmov. Bakteriostatski učinek je zelo kratkotrajen (od 3 do 12 ur). Vnetne spremembe v predelu membran, ki mejijo na cervikalni kanal, jih vedno najdemo prej kot v resicah posteljice. Zaradi nizke virulence večine oportunističnih mikroorganizmov ostanejo plodove membrane navzven nedotaknjene. Hkrati so membrane prepustne za številne oportunistične mikroorganizme, zato lahko pride do okužbe ploda tudi s celim plodovim mehurjem. Povzročitelj prodre v amnijsko tekočino, pride do njenega intenzivnega razmnoževanja in kopičenja. Nastane žarišče okužbe, plod pa je v okuženem okolju. Tako imenovani infekcijski sindrom amnijska tekočina.
Okužba ploda nastane z zaužitjem in aspiracijo okužene vode, kar vodi do pojava pri novorojenčku. znaki intrauterine okužbe(pljučnica, enterokolitis, vezikuloza, omfalitis, konjunktivitis itd.). Hkrati mikroorganizmi, ki se širijo skozi membrane ali med njimi, dosežejo bazalno ploščo posteljice. (deciduitis). Horionska plošča in elementi popkovine se okužijo ob stiku z okuženo amnijsko tekočino. Nadaljnje širjenje vnetne reakcije vodi v razvoj horionitisa (placentitis), kar se kaže z levkocitno infiltracijo interviloznega prostora in endovaskulitisom v horionski plošči. Vaskulitis v deciduu, steblu in terminalnih resicah vodi do obliteracije žil, do pojava srčnih infarktov, kalcifikacije, masivnih fibrinoidnih usedlin, ki se lahko kažejo kot « prezgodnje zorenje posteljica."
Manifestacije sindroma "okužbe amnijske tekočine" poleg horionamnionitisa vključujejo polihidramnij, ki ga lahko odkrijemo pri 5,5-63,6 % bolnic že ob koncu prvega trimesečja nosečnosti. Razlog za njegov razvoj je sprememba razmerja med procesi proizvodnje in resorpcije amnijske tekočine s celicami amnijskega epitelija v ozadju amnionitisa. oligohidramnij pri intrauterini okužbi je običajno sekundarna in je manifestacija okvare ledvic (zmanjšana diureza s placentno insuficienco) oz. sečila plod (obstruktivna hidronefroza).
Oblikovanje placentna insuficienca. V nastanku simptomatskega kompleksa placentne insuficience pri IUI imajo glavno vlogo vaskularne motnje (vaskulitis in tromboza žil fetalnega dela posteljice v ozadju horionitisa (placentitis). Spremembe morfofunkcionalnega stanja celice Pomembne so tudi membrane zaradi aktiviranja procesov lipidne peroksidacije v ozadju placentitisa.Glavne manifestacije placentne insuficience so kronična hipoksija ploda in intrauterino zaostajanje v rasti, ki je glede na čas okužbe simetrična (okužba pred zaključkom placentacije) ali asimetrična.
Tipična manifestacija intrauterine okužbe je spontani splav nosečnost. V 70 % opazovanj se začne spontana prekinitev nosečnosti v poznejših fazah in prezgodnji porod prezgodnja ruptura plodov
školjke in le v 30% - s povečanjem kontraktilne aktivnosti maternice. Prezgodnji razvoj delovna dejavnost in nepravočasne rupture membran so posledica delovanja bakterijskih fosfolipaz, ki sprožijo prostaglandinsko kaskado in škodljivega učinka vnetnih toksinov na membrane.
Zaradi dejstva, da fosfolipaze gram-negativnih bakterij prispevajo k uničenju površinsko aktivne snovi v pljučih ploda, se novorojenček razvije motnje dihanja. Tako je zgrajeno naslednje zaporedje razvoja naraščajoče okužbe: kolpitis, cervicitis - okužba amnijske tekočine - poškodba epitelija plodovnice - membranitis - amnionitis horionske plošče - perivaskulitis popkovine - poškodba dihalnih poti , pljuča, prebavni trakt in koža - prenatalna smrt ploda.
Med mikrobiološkim pregledom žensk skupin povečano tveganje Razvoj IUI bakterijska etiologija Ugotovljena je bila identiteta vrstne sestave mikroflore urogenitalnega trakta žensk in mikroorganizmov, izoliranih od njihovih otrok. Pri novorojenčkih s kliničnimi manifestacijami IUI opazimo masivno sejanje predvsem v notranjih votlinah (želodčna vsebina, bris iz nazofarinksa). Najpogosteje ostanejo kulture brisa z materine površine posteljice in popkovnične krvi
so sterilni, plodovnica in plodna površina posteljice pa imata najvišji rezultat kolonizacija mikrobov. To dokazuje pretežno ascendentno pot okužbe ploda in vodilno vlogo amnijske tekočine pri okužbi ploda.
Za hematogeni okužba ploda je najbolj značilna za prisotnost žarišča v materinem telesu, ki se nahaja ekstragenitalno. Povzročitelj, ki razbije placentno pregrado, prodre v krvni obtok ploda. Pri hematogeni okužbi se pogosto pojavi generalizirana lezija fetalnega telesa - intrauterina sepsa. Vse resnične prirojene virusne okužbe, mikoplazmoza, klamidija, pa tudi tako specifične intrauterine okužbe, kot so listerioza, sifilis in toksoplazmoza, imajo transplacentalno pot okužbe.
Za hematogeno pot je značilna prevlada vaskulitisa posteljice maternice, nato - razvoj interviluzitisa, vaskulitisa horionske plošče, nato - flebitisa in endarteritisa popkovine, okužbe jeter, možganov, poškodb drugi organi ploda - predporodna smrt.
Za izvedbo transdecidualno (transmuralno) pot okužbe zahteva prisotnost žarišča okužbe pod endometrijom. Podobna pot okužbe ploda se najpogosteje pojavlja pri bolnikih, ki so imeli gnojno-vnetne bolezni spolnih organov.
Z padajoče z intrauterino okužbo, pri kateri pride do prodiranja patogena v plodovo jajčece skozi jajcevodov, v klinični praksi je treba obravnavati bolnike z akutno kirurško patologijo organov trebušna votlina, akutni ali kronični salpingooforitis gonorejske, mikoplazmalne ali klamidijske etiologije. Klasičen primer je akutni apendicitis, medtem ko mehanizem poškodbe ploda spominja na ascendentno okužbo.
Imunski sistem ploda
Zreli imunski odziv vključuje zapleteno zaporedje interakcij med več vrstami celic. Proces zorenja posameznih celic, ki sodelujejo pri imunskem odzivu, se začne v zgodnjih fazah plodovega življenja. Progenitorne celice človeškega imunskega sistema se proizvajajo v kostnem mozgu in jetrih ploda. Markerje histokompatibilnosti in antigene, značilne za T- in B-limfocite, lahko odkrijemo na limfocitih že v 8-10 tednih gestacije. Ko celice imunskega sistema dozorevajo na makrofagih, pa tudi na T- in B-limfocitih, se pojavlja vse večje število receptorjev in markerjev histokompatibilnosti, vendar se polno zorenje zaključi šele približno 2 leti po rojstvu.
V tipičnih primerih lahko opazimo odzive na povzročitelje okužb, ki prehajajo skozi posteljico že v drugi polovici nosečnosti. Ta vrsta imunskega odziva se običajno kaže v obliki tvorbe protiteles razreda IgM, lahko pa nastanejo tudi protitelesa razreda IgG. Identifikacija imunskega odziva ploda v obliki protiteles IgG je težja zaradi prisotnosti pasivnih materinih protiteles IgG.
Materina protitelesa IgG začnejo prehajati skozi posteljico okoli sredine nosečnosti. Med porodom je koncentracija IgG v krvi otroka (predvsem materinih imunoglobulinov) enaka ustrezni koncentraciji v krvi matere ali jo celo presega. To pomeni, da ima otrok vsa protitelesa IgG, ki so nastala v materinem telesu. Materina protitelesa IgA in IgM ne prehajajo skozi posteljico, in če se pri otroku odkrijejo protitelesa teh razredov, to pomeni, da so nastala v otrokovem telesu.
Tvorba protiteles IgA pogosto ni popolnoma vzpostavljena do trenutka poroda. Pokazalo se je, da se lahko popoln razvoj tega sistema nadaljuje v prvih sedmih letih življenja. Tako je glavni vir imunosti pri plodu prenos materinih protiteles IgG skozi posteljico, čeprav je njegov imunski sistem že v dokaj zgodnji fazi razvoja sposoben razviti lastno zaščito.
Težave pri preučevanju in interpretaciji rezultatov študij humoralne in celične imunosti pri materi in plodu so privedle do iskanja novih rešitev za oceno imunoreaktivnosti.
v ozadju nalezljivega procesa med nosečnostjo. Tako smo ovrednotili številne pro- in protivnetne citokine (interferoni, interlevkini, faktor nekroze tumorja) v različnih obdobjih gestacije pri plodu, materi in novorojenčku. Ker so citokini in interferoni univerzalni regulatorji vseh imunskih reakcij, tako celičnih kot humoralnih, njihova študija omogoča rešitev najpomembnejšega kliničnega problema - ali obstaja okužba pri plodu in ali je potrebno predpisati zdravljenje? Dokazano je, da zmanjšanje ravni interlevkina-4 v kombinaciji s povečanjem koncentracije gama-interferona in faktorja tumorske nekroze v krvi matere kaže na prisotnost intrauterine okužbe v 86,4%. Takšne študije omogočajo neinvazivno oceno tveganja okužbe pri novorojenčku.
Patogeneza. V patogenezi intrauterine okužbe ploda je pomembna vloga neposredne interakcije patogena in ploda. Obseg poškodb, odkritih med intrauterino okužbo, je zelo širok in je odvisen od značilnosti morfogeneze in odzivov ploda v določenem obdobju intrauterinega razvoja, specifičnih lastnosti in trajanja škodljivega faktorja.
Razmerje med virulenco patogena in resnostjo poškodbe ploda ni vedno neposredno sorazmerno. Pogosto izbrisani puščajoči oz blaga okužba pri materi, ki jo povzročajo toksoplazma, listerija, mikoplazme, klamidija, virusi ali glive iz rodu Candida lahko povzroči smrt ali rojstvo ploda hudo bolan otrok. To dejstvo je posledica tropizma patogenov na določena embrionalna tkiva, pa tudi dejstva, da fetalne celice z visoko presnovno aktivnostjo predstavljajo ugodno okolje za razmnoževanje mikrobov.
Škodljivi učinek bakterijskega povzročitelja okužbe se lahko uresniči z razvojem destruktivnega vnetni proces v različnih organih s tvorbo strukturne ali funkcionalne okvare in z neposrednim teratogenim delovanjem s tvorbo trajnih strukturne spremembe v obliki razvojnih napak. Virusni povzročitelji običajno povzročijo smrtonosne ali razvojne motnje z zaviranjem mitotične celične delitve ali z neposrednimi citotoksičnimi učinki. Popravite procese, ki se razvijejo po vnetju
Jem, pogosto vodijo do skleroze in kalcifikacije tkiv, kar moti tudi proces histogeneze.
Obdobje embriogeneze zajema prve 3 mesece nosečnosti, najbolj občutljiva faza na učinke škodljivih dejavnikov pa je prvih 3-6 tednov organogeneze (kritično obdobje razvoja). Med implantacijo se občutljivost na delovanje škodljivih dejavnikov znatno poveča. Za infekcijske embriopatije, ki se pojavijo v tem času, je značilen pojav deformacij (teratogeni učinek), manj pogosto opazimo embriotoksične učinke. Najprej so prizadeta tkiva, ki so bila v času delovanja sredstva v procesu aktivne diferenciacije. Pri različna telesa obdobja zaznamkov ne sovpadajo v času, zato bo trajanje izpostavljenosti škodljivemu sredstvu odvisno od množice lezij.
Z začetkom zgodnjega fetalnega obdobja plod razvije specifično občutljivost na povzročitelje intrauterinih okužb. Fetalne lezije, ki se pojavijo po 13 tednih, se imenujejo "fetopatije". Pri fetopatiji septične etiologije je možna nastanek malformacij. Morfološka osnova za to so alterativni in proliferativni procesi, ki vodijo v obliteracijo ali zožitev naravnih kanalov in odprtin. Takšne spremembe vodijo do kršitve nadaljnjega razvoja že oblikovanega organa. Torej lahko okužba sečil privede do hidronefroze, prenesenega meningoencefalitisa - do hidrocefalusa v ozadju zožitve ali obliteracije Sylvijevega vodovoda.
Ob okužbi po 27 tednih gestacije se plod pridobi sposobnost specifičnega odziva na vnos povzročitelja okužbe z infiltracijo levkocitov, humoralnimi in tkivnimi spremembami. Škodljivi učinek povzročitelja okužbe se v tem primeru uresniči v obliki funkcionalnih okvar.
Prav tako je treba opozoriti, da so pomembne povezave v patogenezi IUI zastrupitev s presnovnimi produkti povzročitelja okužbe, hipertermija in hipoksemija. Vpliv zgornjih dejavnikov na intrauterini plod se kaže z zamudo pri rasti in diferenciaciji pljuč, ledvic in možganov, tudi če ni drugih manifestacij intrauterine okužbe.
Klinični znaki intrauterine nalezljive bolezni pri novorojenčku ali so prisotne že ob rojstvu ali se manifestirajo
lyatsya v prvih 3 dneh življenja (najpogosteje 1.-2. dan). Pri okužbi v poporodnem obdobju se simptomi nalezljivega procesa odkrijejo pozneje. Daljša inkubacijska doba je možna pri intrauterini okužbi (»pozni« meningitis, osteomielitis, klamidijske lezije itd.) ali, nasprotno, zgodnje manifestacije bolnišnične okužbe (zlasti pri nedonošenčkih).
Najpogostejša klinična manifestacija bakterijske intrauterine okužbe pri novorojenčkih v prvih dneh življenja je t.i. infekcijski sindrom. Tak otrok ima skupno klinični simptomi, ki odraža znake zastrupitve in se izraža v splošni letargiji, zmanjšanem mišičnem tonusu in refleksih (zlasti sesalni refleks), pri regurgitaciji, zavračanju dojk. S strani srčno-žilnega sistema- gluhost srčnih tonov, spremembe v EKG hipoksične narave. Opažena bledica kožo, kršitev ritma in pogostosti dihanja, napadi cianoze. Okužba lahko povzroči razvoj septičnega procesa, pri izvajanju katerega sta pomembna stanje novorojenčka v prvih urah življenja in odmerek povzročitelja. Prezgodnje rojstvo, motnje dihanja in hemodinamike, intrakranialna poškodba, hipoksija prispevajo k zmanjšanju odpornosti novorojenčkovega telesa in so ugodno ozadje, na katerem se okužba izrazi in pridobi značaj septičnega procesa.
Specifične manifestacije intrauterinih okužb pri novorojenčkih so različne - od blagih lokalnih oblik do hudih septičnih.
Klinične manifestacije prirojenih bakterijskih ali mikotičnih kožnih lezij pri novorojenčku so lahko vezikulopustuloza. Odstotek pozitivni rezultati mikrobiološka študija vsebine veziklov, odvzetih takoj po rojstvu otroka, je nizka, zato je sporno, ali "aseptične" mehurčke pripisati prirojeni okužbi ali jo obravnavati kot manifestacijo bakterijske alergije s pojavom izpuščaja na koža. Prava (mikrobiološko potrjena) vezikulopustuloza se kaže pri prenatalno okuženih otrocih, običajno do konca 1. in 2. dneva življenja, povzročitelji pa so najpogosteje streptokoki.
ki skupine B in D, Escherichia, kvasovke podobne glive (Ankirskaya A.S. et al., 1989).
Konjunktivitis, rinitis in otitis, pojavil na 1.-3. dan življenja, je lahko tudi manifestacija intrauterine okužbe. Pri prirojenem konjunktivitisu je poleg mikrobiološke preiskave očesnega izcedka na oportunistične mikroorganizme potrebno odvzeti bris za preiskavo na gonokok.
Intrauterina pljučnica- najpogostejša oblika prirojenih okužb novorojenčka. Pri otrocih od trenutka rojstva opazimo znake odpovedi dihanja: zasoplost, cianoza, pogosto dolgočasnost tolkalnega zvoka in majhne brbotajoče mokre hripanja. Rentgenski pregled, opravljen v prvih urah življenja, potrjuje prisotnost žarišč pljučnice. Prirojena aspiracijska pljučnica se lahko pojavi tudi 2. ali 3. dan življenja. V mikrobiološki študiji aspirata iz traheobronhialnega trakta pri novorojenčkih z aspiracijska pljučnica Najpogosteje izoliramo gramnegativne bakterije, pri bolnišnični neonatalni pljučnici pa Staphylococcus aureus. Potek prirojene pljučnice je hud, saj se zaradi aspiracije velika področja pljuč (spodnji in srednji reženj) izklopijo iz dihanja zaradi bronhialne obstrukcije z aspiracijskimi masami - okuženo plodovnico, ki vsebuje primesi mekonija, plodove kože. tehtnice.
Enterokolitis pri novorojenčkih je lahko tudi v naravi intrauterine okužbe, ko povzročitelj prodre skupaj z amnijsko tekočino v prebavila. Za prirojeni enterokolitis so značilne naslednje klinične manifestacije: počasno sesanje, regurgitacija, napenjanje, povečanje jeter in vranice, razširitev venske mreže sprednjega trebušna stena, pogosto tekoče blato. Dispeptični simptomi se običajno pojavijo na 2-3 dan življenja. Pomemben je mikrobiološki pregled črevesne vsebine (znaki kršitve tvorbe črevesne mikrocenoze - kvantitativna prevlada Klebsiella, Proteus, Pseudomonas aeruginosa).
Poraz centralne živčni sistem z IUI pri novorojenčkih je lahko tako primarna (meningitis, encefalitis) kot sekundarna zaradi zastrupitve. Penetracija vznemirja-
la v možganih ploda se najpogosteje pojavlja vzdolž cerebrospinalnih poti, zato se okužba razvije v membranah glave in hrbtenjača in teče v obliki meningitis in meningoencefalitis. Obstajajo tudi spremembe v horoidnih pleksusih stranskih prekatov možganov, ki jih lahko spremlja razvoj prirojenega hidrocefalusa.
Sepsa pri novorojenčku je zaradi nizke reaktivnosti njegovega telesa težko diagnosticirati. Na začetku bolezni so lahko klinične manifestacije blage, lahko so le znaki splošne zastrupitve, brez očitnega žarišča okužbe (sindrom "okužbe"). Pozorni moramo biti na simptome, kot so letargija, slabo sesanje, regurgitacija, zapoznelo okrevanje ali sekundarna izguba teže, zapoznelo celjenje popkovne rane, razvoj omfalitisa. Tipični simptomi infekcijske zastrupitve pri novorojenčku so motnje dihal in presnove tkiv. Obstaja bledo cianotična, s sivkastim odtenkom, barva kože z izrazitim žilnim vzorcem (mramornost kože). Zastrupitev spremlja kršitev izločevalne funkcije jeter, razvoj dolgotrajne zlatenice. Simptomi sepse vključujejo tudi povečanje vranice in perifernih bezgavk. Informativni znaki so edem podkožno tkivo, hipokromna anemija, motnje v delovanju ledvic in jeter, presnova vode, soli in beljakovin (hipoproteinemija) (Ankirskaya A.S. in
et al., 1989).
Upoštevati morate tudi nespecifične manifestacije intrauterina okužba. Pri novorojenčkih te skupine so prilagoditvene reakcije tako pomembne pomembnih sistemov kot centralni živčni, respiratorni, kardiovaskularni, endokrini in imunski. Pogosto je v prvi minuti po rojstvu nizka ocena po Apgarju. Pogosto se v zgodnjem neonatalnem obdobju pojavijo neuspehi prilagajanja v obliki hipoksičnega sindroma, sindroma respiratornih in srčno-žilnih motenj, nadledvične in možganske patologije. Upoštevati je treba možnost takšnih manifestacij, kot so prirojena podhranjenost, edematozni sindrom, hiperbilirubinemija, krvni sindrom DIC.
PRENATALNA DIAGNOSTIKA NOTRANJIH OKUŽB
Glede na nespecifičnost kliničnih manifestacij te patologije je njena prenatalna diagnoza najtežja.
Najbolj racionalna je postopna diagnoza intrauterinih okužb.
Na prva stopnja na podlagi zbiranja anamnestičnih podatkov in splošnega kliničnega pregleda določimo skupino z visokim tveganjem za razvoj intrauterinih okužb. Ta skupina vključuje bolnike:
Ekstragenitalna žarišča okužbe, zlasti pri poslabšanju infekcijskega procesa med nosečnostjo, pa tudi pri tistih, ki so med nosečnostjo doživeli akutne respiratorne virusne okužbe;
Z zgodnji začetek spolno življenje in pogosta menjava spolnih partnerjev, ki so imeli epizode urogenitalnih okužb;
Tisti, ki so imeli vnetne bolezni maternice in njenih dodatkov, kolpitis, spolno prenosljive bolezni;
Umetna prekinitev nosečnosti z zapletenim potekom obdobja po splavu;
Z spontana prekinitev nosečnost kadar koli v zgodovini;
Z zapletenim tečajem poporodno obdobje po prejšnjih porodih;
Z nalezljivimi in vnetnimi boleznimi spolnih organov (kolpitis, bakterijska vaginoza) med nosečnostjo;
C istmiko-cervikalna insuficienca;
S kliničnimi znaki polihidramnija ali fetoplacentarne insuficience.
Na druga stopnja skozi celovito ultrazvočni pregled identificirati ehografske markerje intrauterinih okužb, pa tudi znake fetoplacentne insuficience in oceniti njeno resnost.
Sonografske znake, ki označujejo IUI, lahko razdelimo v naslednje skupine.
1. Patologija amniona in horiona: - polihidramnij ali oligohidramnij (mogoče diagnosticirati od konca prvega trimesečja nosečnosti);
Hiperehogena suspenzija v amnijski tekočini;
Amnijski trakovi;
Patologija viloznega horiona - hipoplazija resic (mogoče je diagnosticirati med nosečnostjo do 8-9 tednov in se kaže z redčenjem horiona po celotnem obodu do 1-3 mm, zmanjšanjem njegove ehogenosti, prekinitve in gladkosti zunanjega obrisa);
Placentitis, katerega znaki so edem/debelitev (71,8%), heterogena ehogenost parenhima posteljice, odebelitev/podvojitev konture bazalne plošče, zamegljenost meja lobulov, neenakomerno širjenje interviloznih prostorov in subhorionskega prostora ;
Prezgodnje zorenje posteljice.
2. Abdominalni in podkožni edem:
Neimunska kapljica (podkožni edem in plevralni in/ali perikardni izliv ali ascites);
Hidrotoraks;
Dvostranski plevralni izliv.
3. Kalcifikacije v notranjih organih ploda:
Kalcifikacije periventrikularne regije;
kalcifikacije črevesja;
Parenhimske kalcifikacije jeter/vranice.
4. Sprememba ehogenosti notranji organi plod:
Hiperehogeno črevesje (znak ima diagnostično vrednost po 16 tednih nosečnosti);
Črevesna pnevmatoza (odkrita v 25% primerov z IUI);
mehurčki plina v žolčniku;
Hiperehogene velike ledvice normalne velikosti Mehur;
Dvostransko povečanje ehogenosti pljuč (v kombinaciji z rahlim plevralnim izlivom in polihidramnijem je znak intrauterine pljučnice).
5. Strukturne napake (malformacije notranjih organov ploda).
6. Hepatomegalija in splenomegalija.
Odkrivanje ehografskih markerjev IUI ne more služiti kot osnova za diagnozo. Opazili smo, da s kombinacijo treh ehografskih znakov in več verjetnost intrauterine okužbe pri novorojenčku doseže 80%.
Pri ocenjevanju fetometričnih parametrov se opravi diagnoza sindroma zaostanka rasti ploda (FGR) in določi njegova oblika. Dopplerjeva študija pretoka krvi v žilah fetoplacentarnega kompleksa omogoča odkrivanje motenj, ki se pri IUI odkrivajo predvsem v fetalno-placentalnem krvnem obtoku. Kardiotokografski pregled omogoča diagnosticiranje znakov razvoja hipoksije ploda.
Vzporedno z ultrazvočna diagnostika opraviti celovit pregled z uporabo sodobnih laboratorijske metode raziskave za odkrivanje povzročiteljev nalezljivih bolezni v ženskem telesu.
1. Encimski imunski test, ki temelji na določanju IgM in IgG, specifičnih za določeno okužbo, ali antigenov ustreznih patogenov.
2. Metoda molekularne hibridizacije (identifikacija fragmentov DNA ali RNA patogenih celic).
3. Metoda ELISA (določanje monoklonskih protiteles v telesnih tekočinah in medijih s testnim sistemom).
4. bakterioskopski pregled nativnih in po Gramu obarvanih brisov iz sečnice, cervikalni kanal in vagino.
5. Bakteriološka preiskava s posejanjem vsebine cervikalnega kanala, sečnice in nožnice na tekoča in trdna gojišča za kvantificiranje predstavnikov aerobnih in anaerobnih okužb ter njihove občutljivosti na antibakterijska zdravila.
6. Pregled strganja iz cervikalnega kanala s polimerazno verižno reakcijo za identifikacijo povzročiteljev spolno prenosljivih bolezni.
Na tretja stopnja po uporabi posrednih diagnostičnih metod in pridobitvi podatkov, ki kažejo na prisotnost intrauterine okužbe, je mogoče uporabiti metode za neposredno diagnozo IUI v materialu, pridobljenem z biopsijo horionskih resic, amniocentezo in kordocentezo.
Za diagnozo intrauterinih okužb v I trimesečje nosečnost je najbolj priročna aspiracija transcervikalna biopsija horionskih resic. Proizvedeno v 6 do 10 tednih nosečnosti pod nadzorom ultrazvoka. Nastali biopsijski vzorec se podvrže bakteriološkim in virološkim študijam, opravi se tudi kariotipizacija. Pri
pri odkrivanju intrauterine okužbe je treba zastaviti vprašanje prekinitve nosečnosti, saj za okužbo v zgodnji datumi za katero je značilno nastanek malformacij ploda.
Od 16. tedna nosečnosti in vseskozi II trimesečje Uporablja se za diagnosticiranje intrauterine okužbe amniocenteza. Operacija se izvaja v aseptičnih pogojih transvaginalno (skozi sprednji oz zadnji forniks vaginalni ali transcervikalni) ali transabdominalni dostop (uporablja se pogosteje). Pod nadzorom ultrazvoka se opravi punkcija amnijske votline v žepu amnijske tekočine brez zank popkovine in majhnih delov ploda. Za študijo se odvzamejo trije vzorci amnijske tekočine s skupno prostornino 24 ml, ki se nato podvržejo mikrobiološkim, biokemijskim in genetskim študijam.
Obstajajo številni testi za odkrivanje intrauterinih okužb v amnijski tekočini: plinsko-tekočinska kromatografija amnijska tekočina za določitev organskih kislin (acetat, sukcinat, butirat, oksaloacetat itd.), ki je specifična za prisotnost povzročitelji infekcij v amnijski tekočini.
Uporabljajo tudi bakterioskopijo nativnih in po Gramu obarvanih brisov amnijske tekočine, ki jih posejejo na tekoče in trdne medije. Odkrivanje v kulturi etiološko pomembnih mikroorganizmov v količini, ki presega 5 × 10 2 CFU / ml, je diagnostično merilo intrauterina okužba.
Pri diagnostiki virusnih intrauterinih okužb se uporabljata gojenje virusnih povzročiteljev na piščančjih zarodkih in polimerazna verižna reakcija.
Pomembno vlogo imajo serološke raziskovalne metode, med katerimi je najbolj občutljiva in specifična določanje monoklonskih protiteles s testnim sistemom ELISA.
Aktivnost se ugotavlja alkalna fosfataza levkocitov popkovnične krvi, štetje števila trombocitov (trombocitopenija pod 150-10 9/l velja za znak okužbe), razmerje mladih oblik levkocitov in nevtrofilcev ter določanje radioizotopov β-laktamaze (značilno za okužbo z β- mikroorganizmi, ki proizvajajo laktamazo). Kri je podvržena tudi bakteriološkim, virološkim in imunološkim študijam.
Predklinična diagnoza IUI temelji predvsem na ciljnem mikrobiološkem pregledu novorojenčkov (takoj po rojstvu) in histološkem pregledu posteljice pri nosečnicah s povečanim tveganjem okužbe pri plodu.
V nasprotju z mikrobiološkimi in histološkimi metodami imunološki pregled novorojenčkov ob rojstvu, zlasti določanje glavnih razredov imunoglobulinov v popkovnični krvi, ni dovolj informativen za predklinično diagnozo IUI. To je posledica dejstva, da so enake vrednosti imunoglobulinov G, M, A zabeležene pri novorojenčkih s kliničnimi manifestacijami okužbe in brez njih. Povišana raven IgM v popkovnični krvi odraža antigensko stimulacijo, ki se je zgodila v predporodnem obdobju, vendar ne kaže vedno na prisotnost infekcijskega procesa.
ZNAČILNOSTI POSAMEZNIH NOZOLOŠKIH OBLIK INTRAuterinih okužb
Citomegalovirus
Citomegalovirus (CMV) je virus iz družine herpes virusov, ki vsebuje DNK, je vseprisoten in se lahko prenaša z različnimi telesnimi izločki (kri, urinom), najpogosteje pa s spolnim stikom. Pri odraslih okužba praviloma poteka brez očitnih kliničnih manifestacij, možen pa je tudi potek, podoben mononukleozi.
Okužba s CMV se pojavi pri tesnem stiku z okuženo osebo ali z naraščajočo okužbo z matere na otroka. Virus se občasno izloči s slino, urinom in genitalnim izločkom ter se prenaša s poljubljanjem, spolnim odnosom ali drugim stikom.
Citomegalovirus, ki je enkrat vstopil v človeško telo, se po primarni okužbi ne izloči v zunanje okolje, ampak v njem vztraja vse življenje. Dolgotrajen latentni potek okužbe olajša znotrajcelični obstoj virusa, kjer je zanesljivo zaščiten pred delovanjem specifičnih protiteles. Serološke študije, opravljene v Rusiji, so pokazale, da ima 90 % nosečnic protitelesa proti CMV, kar kaže na izjemno visoko
com raven prenašanja virusa. Med nosečnostjo se ustvarijo resnični pogoji za reaktivacijo okužbe, ki je povezana z gestacijskimi značilnostmi delovanja imunskega sistema (stanje fiziološke imunosupresije).
Verjetnost intrauterine okužbe ploda z latentnim potekom okužbe je praktično odsotna, z njeno reaktivacijo je 0,5-7%, pri primarni okužbi pa presega 40%. Skupna incidenca prenatalne okužbe s CMV je 5-20 na 1000 živorojenih otrok. Prenatalna okužba s citomegalovirusom je pri seropozitivnih ženskah 5 %, do 20 % okužb se pojavi med porodom, še 10 % otrok se okužbo okuži v zgodnjem poporodnem obdobju – največkrat od matere, preko kontaminiranega materinega mleka.
Najpogostejša pot okužbe je transplacentalna, redkeje plod pogoltne okuženo plodovnico ob prisotnosti placentitisa in horioamnionitisa.
Virus lahko okuži kateri koli organ ploda, vključno s centralnim živčnim sistemom. Za okužbo epitelijskih celic je značilen razvoj velikih intranuklearnih vključkov (citomegalični vključki). V prizadetih tkivih opazimo citolizo z območji žariščne nekroze in pretežno mononuklearne vnetna reakcija. Celjenje vodi do fibroze in kalcifikacije, zlasti v subependimalni membrani možganskih ventriklov in v jetrih. Težka možganski zapleti, vključno z mikrocefalijo in kalcifikacijami, so običajno posledica intrauterine okužbe v prvih 3–4 mesecih nosečnosti, ko je ventrikularni sistem v razvoju.
V zvezi s porazom v zgodnjih fazah gestacije nastanejo embriopatije, razvijejo se hude trofične motnje gestacijsko vrečko, pride do smrti zarodka ali ploda, nosečnost se konča s spontanim splavom. Za mrtvorojene plodove so značilne hude možganske motnje, vključno z mikrocefalijo, hidrocefalusom in kalcifikacijami, porencefalijo, cistofibrozo trebušne slinavke, cirozo jeter, atrezijo žolčevodov, kortikalno displazijo ledvic.
V kasnejših obdobjih se oblikujejo fetopatije s fetoplacentno insuficienco, intrauterino zaostajanje v rasti in stigme disembriogeneze. Novorojenčki imajo epitelijske lezije žleze slinavke, zvite tubule ledvic, bronhijev, žolča
kanalov. Glede na obsežno (sonografsko, doplerometrično in kardiotokografsko) študijo (hormoni - placentni laktogen, progesteron, estriol, kortizol; vsebnost AFP) - znake intrauterinega trpljenja ploda najdemo pri 33,9 %.
Klinične manifestacije. 90-95 % dojenčkov, okuženih s CMV v maternici, ob rojstvu nima nobenih simptomov. Večina se jih razvija normalno, vendar natančno spremljanje v daljšem časovnem obdobju kaže, da se pri 10–30 % otrok pozneje pojavijo simptomi manjših nevroloških poškodb – živčna gluhost, zakasnjen razvoj ali blaga duševna zaostalost. Poleg tega je možna specifična kršitev funkcije celične imunosti - zaviranje aktivnosti T-pomagalcev, povečanje vsebnosti IgM in IgG.
Pri majhnem deležu otrok s kliničnimi znaki okužbe se ti gibljejo od intrauterina zamuda rast (najpogosteje kot povečanje jeter in vranice) ali vpletenost v proces ločenega organa do hude, generalizirane, življenjsko nevarno bolezen, ki je redka.
Številne ekstragenitalne manifestacije prirojene okužbe s citomegalovirusom (hepatitis, trombocitopenija, hemolitična anemija in pljučnica) izginejo v določenem obdobju brez zdravljenja. Nevrološka poškodba je nepopravljiva, čeprav je stopnja invalidnosti različna. Večina otrok s prirojenimi okužba s citomegalovirusom otroci, ki so rojeni s simptomi okvare živčnega sistema, trpijo za resnimi nepopravljivimi nevrološkimi motnjami, vključno s cerebralno paralizo, epilepsijo in živčno gluhostjo. Horioretinopatija je precej pogosta. Redko povzroči kakršno koli okvaro vida in je priročna diagnostična značilnost pri sumu na prirojene okužbe, čeprav se ne razlikuje od horioretinopatije zaradi toksoplazmoze. Smrtnost pri prirojeni citomegaliji je 20-30%.
Preprečevanje in zdravljenje. Do danes niso bila razvita učinkovita varna cepiva ali pripravki že pripravljenih specifičnih monoklonskih protiteles. Preventivni ukrepi so zmanjšani na izolacijo okuženih novorojenčkov in izključitev stika teh novorojenčkov s seronegativnimi nosečnicami. Osebje, ki skrbi zanje, dela v rokavicah in sekundo
kopalni plašč. Kot pasivno profilakso lahko uporabite vnos pripravkov že pripravljenih protiteles z visoka vsebnost anticitomegalovirusni IgG.
Kljub nedavnemu napredku pri zdravljenju okužb, ki jih povzročajo α-herpesvirusi (virus herpes simplex in virus varicella-zoster), zdravljenje bolezni β-herpesvirusa ni dokončno razvito. Uporabljata se valaciklovir in ganciklovir, vendar ni zadostnih izkušenj z njuno uporabo pri nosečnicah. Kompleks zdravljenja vključuje uporabo rastlinskih adaptogenov (eleutherococcus, ginseng, matični mleček), vitaminov skupine B (B 1, B 6, B 12) do 14 tednov gestacije.
Od 15-16 tednov se kot metoda paliativnega zdravljenja izvaja tečaj imunoglobulinske terapije z normalnim humanim imunoglobulinom ali pripravki že pripravljenih protiteles z visoko vsebnostjo anti-citomegalovirusnega IgG - imunoglobulinov proti citomegalovirusu. Z uvedbo imunoglobulinskih pripravkov materino telo prejme že pripravljena protitelesa (AT) proti CMV. Abs IgG razreda aktivno prehajajo skozi posteljico in ustvarjajo pasivno imunost pri plodu. V telesu nosečnice protitelesa blokirajo zunajcelično locirane viruse, z njimi ustvarjajo imunske komplekse, spodbujajo izločanje iz telesa in omejujejo širjenje v limfnem in krvnem obtoku. Imunoglobulinsko zdravljenje se izvaja ob upoštevanju tveganja alergijskih, pirogenih reakcij, proizvodnje anti-y-globulinov, poslabšanja okužbe, t.j. v primerih, ko je tveganje za neželene učinke okužbe večje.
Pridobljeni podatki o zmanjšani sposobnosti levkocitov za tvorbo α- in y-interferona pri ženskah z virusnimi okužbami kažejo, da je v kompleksno zdravljenje nosečnic s citomegalovirusno okužbo priporočljivo vključiti imunomodulatorne in interferonske komponente. Uporablja se gensko spremenjeno rekombinantno zdravilo viferon, ki je a2-interferon, povezan z antioksidanti. Ima imunomodulatorne in antioksidativne lastnosti, ki stabilizirajo interferon.
Novost pri zdravljenju okužb s herpesom je uporaba plazmafereze in endovaskularnega laserskega obsevanja krvi (ELOK). Terapevtska učinkovitost plazmafereze in ELOK je posledica učinka razstrupljanja, stimulativnega učinka na
celični in humoralna imunost in reakcije nespecifične rezistence, normalizacija koagulacijskih in agregacijskih lastnosti krvi.
herpetična okužba
Najpomembnejšo vlogo imajo virusi družine herpesviridae. Virus herpes simpleksa (HSV) vsebuje DNK in spada v isto skupino kot CMV, Epstein-Barr virus in virus norice- skodle. Ugotovljena sta bila dva njegova serotipa HSV-1 (orolabialni) in HSV-2 (genitalni), vendar ni popolnega ujemanja med serotipom in lokalizacijo okužbe. Pri 20 % okužb novorojenčkov je povezan z okužbo s HSV-1 genitalij.
Prenaša se virus herpes simpleksa različne poti, najpomembnejša je spolna pot. Poraz virusa genitalnega herpesa se odkrije pri 7% nosečnic. Herpes pri novorojenčkih je zabeležen s pogostostjo 1: 2000-1: 5000, vendar je kljub relativni redkosti neonatalnega herpesa, resnosti njegovih manifestacij in neugodni prognozi za novorojenčka zelo pomembno razviti racionalne pristope k diagnozi. , zdravljenje in zlasti preprečevanje te izjemno resne bolezni.
Pogostost odkrivanja HSV-2 se močno razlikuje glede na številne dejavnike (starost, narava spolne aktivnosti, sociokulturna raven prebivalstva itd.). Tako so pri mladostnikih, mlajših od 15 let, seropozitivni rezultati manj kot 1 %, medtem ko se med bolniki klinik, specializiranih za spolno prenosljive bolezni, gibljejo med 46-57 %. Pri nosečnicah se specifična protitelesa proti HSV-2, na primer v ZDA, odkrijejo v povprečju pri 20-30 % žensk.
Klinične manifestacije primarne okužbe pri materi trajajo 18-22 dni, s povečanjem simptomov v 1. tednu. V naslednjih 2 tednih opazimo asimptomatsko luščenje epitelija, ki ga je poškodoval virus. Skupno trajanje manifestacij je skoraj 6 tednov. Neprimarna genitalna okužba je manj izrazita: trajanje kliničnih manifestacij je krajše (približno 15 dni), asimptomatsko izločanje virusa je manj pogosto, njegovo trajanje pa se zmanjša na 8 dni. Resnost in trajanje kliničnih manifestacij pri relapsih je še manj izrazita, trajanje luščenja poškodovanega epitelija pa je le 4 dni.
Primarni genitalni herpes pri materi in poslabšanje kronični proces so najbolj nevarni za plod. Če je 0,5-1,0% novorojenčkov okuženih intranatalno, potem z akutni potek ali poslabšanje, ki se kaže z vezikularnimi lezijami kože in sluznice genitalij, tveganje okužbe ploda med porodom doseže 40%.
Pri intrauterini okužbi s HSV-2 se v večini primerov okužba ploda pojavi tik pred porodom, dvigne se po rupturi membran (kritično obdobje 4-6 ur) ali med porodom, ko prehaja skozi okužene. porodni kanal(85 %). Prenos okužbe se pojavi tako v prisotnosti lezij na materničnem vratu in vulvi ter pri asimptomatski izolaciji virusa. Z naraščajočo potjo okužbe se patogen pomnoži in kopiči v amnijski tekočini, opazimo polihidramnij. Ko pride do okužbe, se virus lahko širi s kontaktnimi ali hematogenimi potmi. Pri 5% se transplacentalno širjenje pojavi med nosečnostjo.
Poraz posteljice in ploda z okužbo s herpesom se lahko pojavi v kateri koli fazi nosečnosti in povzroči nastanek v plodu prirojene napake razvoj, predporodna smrt, spontani splav ali prezgodnji porod. Okužba v prvem trimesečju vodi do nastanka hidrocefalusa, srčnih napak, anomalij gastrointestinalnega trakta, pogosto pride do spontanega splava, razvije se intrauterino zaostajanje v rasti. V II in III trimesečju infekcijski proces vodi v razvoj hepatospelenomegalije, anemije, zlatenice, pljučnice, meningoencefalitisa, sepse, podhranjenosti. Intrauterina okužba se v pozni nosečnosti manifestira zgodnji razvoj klinična slika neonatalne okužbe (prvi dan) pri otrocih, rojenih tudi kot posledica carski rez. Pogoste manifestacije herpetične okužbe: poškodbe kože, ustne sluznice, horioretinitis.
Okužba s herpesvirusom novorojenčkov se kaže v treh kliničnih oblikah.
Lokalna oblika s poškodbami kože in sluznic- 45 %. Poškodbe kože in sluznic so najpogostejše, a tudi najpogostejše lahka oblika neonatalni herpes. Oči: keratokonjunktivitis in horioretinitis. Koža in ustna sluznica: mehurčki,
eritem, petehije. Če se bolezen ne zdravi, lahko napreduje z razvojem hudih zapletov. Smrtnost je približno 18%.
Lokalna oblika s poškodbo CNS(encefalitis) - 35%. Značilnost: zvišana telesna temperatura, letargija, zmanjšan apetit, depresija ali sindrom vznemirjenosti, tremor, konvulzije. Ugotovljene so izrazite spremembe v cerebrospinalni tekočini. Smrtnost v odsotnosti zdravljenja je več kot 50%.
Razširjena oblika- dvajset %. Pri razširjeni obliki neonatalnega herpesa je običajno v proces vključenih več organov hkrati: jetra, pljuča, koža, nadledvične žleze. Znaki se pojavijo v 1.-2. tednu življenja, vključujejo simptome lokalizirane oblike v kombinaciji z anoreksijo, bruhanjem, letargijo, zvišano telesno temperaturo, zlatenico, motnjami dihanja, krvavitvami, šokom (slika 35). Začetek krvavitve in žilnega kolapsa je lahko nenaden in hitro usoden. Smrtnost v tej obliki je izjemno visoka - 90%. Sodobna antiherpetična kemoterapija lahko bistveno izboljša prognozo, vendar kljub tekočemu zdravljenju ostaja tveganje za dolgotrajne nevrološke motnje precej visoko.
Preživeli otroci imajo v prihodnosti hude zaplete (nevrološke motnje, motnje vida, psihomotorična zaostalost).
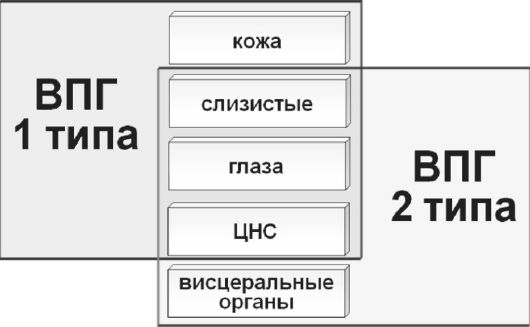 riž. 35. Tkivni tropizem virusov herpesa
riž. 35. Tkivni tropizem virusov herpesa
Preprečevanje, zdravljenje in vodenje nosečnosti. Narava preventivnih in medicinske ukrepe, kot tudi porodniška taktika, je odvisna od vrste, oblike (tipična, atipična, asimptomatska in trajanja poteka) in prisotnosti lezij genitalij, stanja membran.
Pri primarni okužbi v zgodnjih fazah nosečnosti je treba zastaviti vprašanje njene prekinitve. Če se bolezen pojavi pozno ali je bila ženska okužena pred nosečnostjo, preventivni ukrepi vključujejo dinamično ehografsko spremljanje razvoja in stanja ploda, predpisovanje tečajev terapije, vključno s presnovnim kompleksom, stabilizatorji celične membrane, unitiolom. O vprašanju prekinitve nosečnosti se odloča posamezno.
Dokazana korist kompleksno zdravljenje herpetične lezije. Glavna kemoterapija je aciklovir ali valaciklovir. Kemoterapija je možna od prvega trimesečja nosečnosti. Kljub pomanjkanju dokazov o teratogenih in embriotoksičnih učinkih je predpisovanje aciklovirja nosečnicam omejeno zaradi naslednje indikacije: primarni genitalni herpes, ponavljajoči se genitalni herpes (tipična oblika), genitalni herpes v kombinaciji z grozečim splavom ali simptomi IUI. Pri nosečnicah, ki imajo pogoste ponovitve okužbe, se izvaja trajno zdravljenje z aciklovirjem (supresivno zdravljenje). V primeru zapletenega poteka okužbe s herpesom (pljučnica, encefalitis, hepatitis, koagulopatija) se zdravljenje izvaja skupaj s specialistom za nalezljive bolezni.
Hkrati je priporočljivo predpisati imunoglobulinsko terapijo, pripravke interferona, "velike" antioksidante (vitamina E in C). Opozoriti je treba na potrebo po zdravljenju bolezni, povezanih s herpesom (najpogosteje klamidija, mikoplazmoza, trihomonijaza, kandidoza, bakterijska vaginoza). Tako kot za zdravljenje citomegalije sta pri zdravljenju herpesne okužbe našla svoje mesto plazmafereza in endovaskularno lasersko obsevanje krvi. Po kompleksni terapiji se pogostost zapletov pri materi in plodu zmanjša za 2-3 krat.
Porodniško vodenje žensk z genitalnim herpesom je odvisno od njegove oblike in trajanja nosečnosti. V primeru primarne okužbe med nosečnostjo (1 mesec pred porodom ali manj) ali ponovitve (nekaj dni pred porodom) se izvaja kemoterapija,
porod poteka s carskim rezom. Ob prisotnosti genitalnega herpesa v anamnezi pri enem od staršev je pred porodom indicirana študija kulture ali PCR. Če je odgovor negativen - porod skozi porodni kanal.
Kljub ustrezno organizirani porodniški oskrbi trenutno ni pogojev za popolno odpravo prenosa okužbe s HSV z matere na novorojenčka. To je posledica nemožnosti identifikacije vseh žensk z asimptomatsko okužbo z genitalnim herpesom. V zvezi s tem se v 70% prenosa okužbe s herpesom na novorojenčke zgodi ravno od mater z asimptomatskim herpesom.
Rdečke
Vlogo virusa rdečk kot vzroka prirojenih malformacij je leta 1941 prvič prepoznal avstralski oftalmolog Norman Gregg. Prvič je opisal sindrom sive mrene, gluhosti in prirojene srčne bolezni pri otrocih, katerih matere so imele rdečke med nosečnostjo med epidemijo v Sydneyju leta 1940. Virus je bil prvič izoliran v tkivni kulturi leta 1962. Do leta 1969 se je pojavilo učinkovito živo oslabljeno cepivo.
Virus rdečk je virus, ki vsebuje RNA in spada v skupino togavirusov (mikrovirusov). Človek je edini nosilec. Virus rdečk ni odporen na zunanje okolje, se širi s kapljicami v zraku; za okužbo je potreben dolgotrajen stik, en sam stik običajno ni dovolj, a ker je bolezen pogosto asimptomatska, stik morda ni znan.
Velika večina ljudi, ki so zboleli za rdečkami, razvije stabilno imunost, vendar 0,3-4,25 % ljudi ponovno zboli za rdečkami, saj je zaradi manjvrednosti obstoječe humoralne imunosti možna ponovna aktivacija predhodno prenesenih rdečk ali ponovna okužba. Hkrati pa se po mnenju raziskovalcev iz Sankt Peterburga v praksi takšna opažanja dejansko ne pojavljajo, in če je akutna rdečka klinično in serološko izključena, je tveganje za intrauterino okužbo izključeno. Če obstaja visok ali naraščajoč titer protiteles proti antigenu rdečk, je treba določiti specifična protitelesa IgM pri materi, če pa jih odkrijemo, v krvi ploda, pridobljeni s kordocentezo.
Okužba ploda se pojavi le od bolne matere. Ženskam, ki so zbolele za rdečkami, lahko priporočamo nosečnost ne prej kot 6 mesecev po okrevanju. Poraz nastane kot posledica viremije in transplacentnega prodiranja virusa.
Samo klinični simptomi niso dovolj za postavitev diagnoze. Iz istega razloga anamneza rdečk ne kaže na imuniteto. Za dokaz okužbe z rdečkami je potrebna izolacija virusa ali ustrezno serološko testiranje.
Merila za diagnozo nedavne rdečke so:
Izolacija virusa rdečk (običajno iz grla);
Povečanje titra protiteles za 4-krat ali več;
Prisotnost IgM, specifičnega za rdečke, ki se določi šele v 4-6 tednih po primarni okužbi.
Če diagnoza ostaja v dvomih, še posebej, če je prišlo do stika v najzgodnejših fazah nosečnosti, se lahko opravi amniocenteza v 14-20 tednih in poskus izolacije virusa rdečk iz plodovnice, ki bo, če bo uspešen, nakazal vsaj okužba posteljice. Negativni rezultati kulture ne izključujejo okužbe posteljice ali ploda. Najbolj natančna je kordocenteza.
Rdečke pri nosečnici lahko povzročijo naslednje posledice:
Brez vpliva na plod;
Okužba samo posteljice;
Okužba posteljice in ploda (od asimptomatski potek pred porazom mnogih sistemov);
Smrt ploda (spontana prezgodnja prekinitev nosečnosti ali mrtvorojenost).
Okužba ploda lahko sledi okužbi matere v kateri koli fazi gestacije, pri čemer je izid rdečk močno odvisen od gestacijske starosti.
Verjetnost okužbe ploda pred 8 tednom gestacije je 54%, pri 9-12 tednih - 34%, 13-24 tednov - 10-20% in ne več kot 12% - od konca II trimesečja. Viremija pri ženskah v prvih 8 tednih nosečnosti vodi do okužbe posteljice in spontani splav ali mrtvorojenost; ob okužbi sredi nosečnosti se rubeolarna fetopatija pogosteje diagnosticira pri nedonošenčkih; z okužbo z rdečkami v tretjem trimesečju
poteka brez prirojenih malformacij, kot sta kronični encefalitis in produktivni leptomeningitis pri novorojenčkih.
Klinika za prirojene rdečke. Virus rdečk kaže izjemen tropizem za mlado embrionalno tkivo, kar je povezano z embriopatijo pri tej bolezni. Virus rdečk na plod vpliva na več načinov. Dodeli "klasični sindrom prirojenih rdečk" ki vključuje triado najbolj tipičnih razvojnih anomalij: katarakta z zamegljenostjo roženice, srčne napake(prirojene okvare ventrikularnega septuma - rubeolarna embriopatija) in gluhost(krvavitve v mehka tkiva zunanji, srednji in notranje uho). Sindrom prirojene rdečke se pogosto kombinira s produktivno intersticijsko pljučnico z velikansko celično metamorfozo alveolocitov.
Poleg klasičnega obstaja "Napredni sindrom prirojene rdečke" ki poleg treh poimenovanih malformacij vključuje številne druge razvojne anomalije: mikrocefalijo, povečan fontanel, poškodbe možganov, glavkom, razcepljeno nebo, intersticijsko pljučnico, hepatitis, poškodbe vestibularnega aparata, skeletne malformacije, poškodbe tubularnih kosti, hepatosplenomegalija, genitourinarne malformacije organov.
Do 70 % preživelih otrok s serološkimi dokazi o okužbi ob rojstvu je zdravih, vendar v prvih 5 letih življenja več kot 2/3 otrok razvije kakršne koli znake okužbe. Najpogosteje so to manj očitni zapleti, ki jih sestavljata blaga do zmerna gluhost in poškodbe možganov z upočasnjenim psihomotoričnim razvojem. Pozne manifestacije rdečk vključujejo tudi imunološke diskrazije (zakasnitev sposobnosti novorojenčka, da sintetizira lastne imunoglobuline kot odziv na virusno okužbo), izgubo sluha, psihomotorično zaostalost, avtizem, cerebralne sindrome (sklerozirajoči panencefalitis), sladkorno bolezen.
Med neonatalnimi manifestacijami rdečk je najbolj značilna trombocitopenična purpura, ki traja od 2 tednov do 3 mesecev. Tipičen hepatitis z zlatenico, hemolitična anemija z retikulocitozo in deformiranimi eritrociti, nezapiranje sprednje fontanele s pleocitozo cerebrospinalne tekočine, intersticijska pljučnica, poškodba cevastih kosti (odkrita rentgensko in je sestavljena iz izmeničnih in rarefalnih območij zbijanja). Od srčnih napak je najpogostejša
je razcep arterijskega (Botallovega) kanala, pogosto v kombinaciji s stenozo pljučna arterija. Obstajajo tudi stenoza in koarktacija aorte, VSD in ASD, transpozicija velikih žil; napake "modre" vrste so redke.
Najbolj tipična očesna bolezen – katarakta – je posledica neposrednega delovanja virusa rdečk, ki lahko v leči vztraja več let. Katarakta je lahko odsotna ob rojstvu in se pojavi v neonatalnem obdobju. Glavkom je 10-krat manj pogost. Poleg tega je pri rdečkah mogoče odkriti pigmentno retinopatijo, zamegljenost roženice, kratkovidnost in nerazvitost vek.
Najpogostejša napaka pri prirojenih rdečkah je gluhost, pogosto v kombinaciji z vestibulopatijo – okvaro Cortijevega organa.
Čim krajša je gestacijska doba, pri kateri ženske zbolijo za rdečkami, pogosteje se kaže teratogeni učinek virusa. Teratogena nevarnost rdečk v 1. mesecu nosečnosti je 35-50% (po nekaterih poročilih se približuje 100%), v 2. mesecu -
25%, v 3. - 7-10%.
Škodljivi učinek rdečk na plod se ne kaže le v njenem teratogenem učinku. okužba z rdečkami v zgodnje obdobje nosečnosti v 10-40% lahko privedejo do spontanih splavov, v 20% - do mrtvorojenosti, 10-25% otrok, rojenih živi, umre v neonatalnem obdobju.
Bolezen rdečk v prvem trimesečju nosečnosti, ki jo potrdijo klinični, epidemiološki in laboratorijski podatki, je indikacija za njeno prekinitev. Ob stiku nosečnice z bolnikom z rdečkami, najkasneje 10-12 dni, je treba opraviti serološki pregled. Če se seronegativna reakcija nadaljuje, natančno opazovanje in ponovni serološki pregled po 2 tednih, da se odkrije asimptomatska okužba.
Preprečevanje je predvsem s cepljenjem. Cepljenje otrok je potrebno. Nosečnice niso cepljene, ker se uporablja oslabljeno cepivo. živo cepivo teratogenih učinkov ni mogoče izključiti. Priporočljivo je presejanje žensk v rodni dobi na prisotnost protiteles proti antigenom virusa rdečk.
Toksoplazmoza
Toxoplasma gondii spada med protozoje, ki okužijo celice skoraj vseh vrst pri sesalcih. Ta povzročitelj okužbe je razširjen po vsem svetu, prizadene ljudi in živali, vendar se končni cikel razmnoževanja zgodi le v črevesju mačk. Oociste vstopijo v telo osebe, ki uživa zelenjavo ali drugo hrano, onesnaženo z oocistami iz zemlje. Po absorpciji oocist v črevesju se sproščajo trofozoiti. Prodrejo v epitelij, kjer se namnožijo in se nato – skozi limfni in cirkulacijski sistem – razširijo po telesu. V telesu zdravega imunokompetentnega gostitelja je razmnoževanje trofozoitov omejeno z razvojem celičnega imunskega odziva in v manjši meri s proizvodnjo specifičnih protiteles. Nekateri od teh organizmov preprečujejo nastanek tkivnih psevdocist, ki so vmesno kopičenja organizmov, obdanih z zaščitno lupino. V tej obliki ostanejo latentni, vendar sposobni preživetja skozi celotno življenje gostitelja, običajno ne povzročajo pomembnega imunskega odziva. Če je normalna imunost iz nekega razloga zmanjšana, se okužba lahko ponovno aktivira.
Druga pomembna pot okužbe je uživanje surovega ali premalo kuhanega mesa okužene živali. Na ta način se človek najpogosteje okuži ob uživanju jagnjetine ali svinjine. Z ene osebe na drugo se okužba ne prenaša, razen prenosa skozi posteljico z matere na plod med razvojem akutna okužba med nosečnostjo. Ni prepričljivih podatkov o povezavi kronične ali latentne okužbe s ponavljajočimi se splavi.
Pogostost okužbe pri ljudeh T. gondii v kateri koli populaciji je odvisno od podnebja, načina priprave hrane in poleg tega stika z mačkami. Prevalenca zaznavnih protiteles je stabilna
Pogostost prirojene toksoplazmoze je težko določiti, saj je večina okuženih otrok ob rojstvu praktično zdravih, okužba pri materi pa je običajno asimptomatska. Obstajajo dokazi, da večina okuženih otrok pozneje trpi za resni zapleti te okužbe, ki lahko zahteva specializirano dolgotrajno zdravljenje. Teoretično ocenjeno tveganje za prirojeno okužbo, ki temelji na letnih stopnjah serokonverzije pri ženskah v rodni dobi, se giblje od 4 do 50 na 10.000 živorojenih otrok.
Klinične manifestacije okužbe. Klinične manifestacije okužbe pri toksoplazmozi so naslednje.
"Pridobljena toksoplazmoza. V večini primerov okužba ljudi T. gondii je asimptomatska ali neprepoznana. po največ pogosta manifestacija okužba je generalizirana limfadenopatija, ki je, čeprav ne vedno, povezana s slabim počutjem, zvišano telesno temperaturo, vneto grlo, glavobolom, izpuščajem. Včasih hkrati najdemo atipično limfocitozo brez heterofilnih protiteles. Okužba je običajno omejena. V redkih hujših primerih so v infekcijski proces vključeni možgani, miokard, jetra ali pljuča, kar zahteva specifično zdravljenje. Horioretinitis je razmeroma redek in je običajno enostranski. * Prirojena toksoplazmoza. Ko je ženska na samem začetku nosečnosti okužena s toksoplazmozo, je tveganje za prenos na njen plod razmeroma majhno (približno 20 %), vendar lahko pride do okužbe v tem obdobju. hude posledice do smrti ploda. Ob rojstvu se anomalije odkrijejo le pri 10-20 % otrok s prirojeno toksoplazmozo, večina otrok s hudimi motnjami se okuži v zgodnji nosečnosti. Huda intrauterina toksoplazmoza lahko privede do smrti oz
resne anomalije v razvoju ploda, vključno s hidrocefalusom, tvorbo cist s kalcifikacijami ali ekstremno tanjšanjem možganske skorje s kalcifikacijami, glialnimi proliferati, produktivnim endarteritisom, razvojem generaliziranega edema s hidrotoraksom in ascitesom, razširjenim vnetjem in uničenjem tkiv različnih organov. V porodu se odkrije kronični vilusitis, v stromi resic - limfna infiltracija s primesjo plazemskih celic. specifičen znak je odkrivanje patogena v obliki cist ali prosto ležečih oblik pri obarvanju po razmazi-odtiski Romanovsky-Giemsa z materinske površine posteljice ali iz globine reza placentnega tkiva; končna diagnoza temelji na odkrivanju protozojev v intersticijskih psevdocistah pri plodu.
Huda prirojena toksoplazmoza pri novorojenčkih je pogosto generalizirana bolezen, ki se kaže kot anemija, povečanje jeter in vranice, zlatenica, zvišana telesna temperatura in limfadenopatija. Pri natančnem pregledu fundusa večina okuženih otrok pokaže znake obojestranskega horioretinitisa. Prizadeta osrednjega živčevja se lahko kaže kot intrakranialna kalcifikacija, epileptični napadi, hidrocefalus, mikrocefalija ali spremembe cerebrospinalne tekočine (zlasti napredni nivo veverica). Približno 80 % otrok s kliničnimi znaki toksoplazmoze ob rojstvu ima nepopravljivo okvaro možganov, 50 % pa ima okvaro vida. Če mati kasneje v nosečnosti zboli za toksoplazmozo, je verjetnost okužbe ploda večja, vendar se ob rojstvu klinični znaki okužbe večinoma ne kažejo, če pa so, so običajno lokalizirani v zrklo ali centralnega živčnega sistema in pri novorojenčku pogosto ostanejo neopaženi.
Očesni simptomi se postopoma pojavijo pri več kot 80 % okuženih otrok, čeprav jih včasih prepoznamo le pri starejših otrocih ali mladostnikih. Približno 4 otroci v tej skupini trpijo za znatno izgubo vida in enako število za ponavljajočim se aktivnim horioretinitisom z vsaj začasno okvaro vida.
resno nevrološke motnje manj pogosto (<10%), в отдаленном периоде прицельное изучение умственных способ-
Rezultati kažejo poslabšanje rezultatov pri več otrocih. Pogosto pride do delne izgube sluha.
Preprečevanje in zdravljenje nosečnic s toksoplazmozo. Tveganje okužbe s toksoplazmozo lahko zmanjšamo na naslednje načine.
1. Izogibajte se uživanju premalo kuhanega ali surovega mesa, zlasti svinjine ali jagnjetine, in si po ravnanju s surovim mesom temeljito umijte roke.
2. Med brejostjo se ni treba izogibati stiku z domačo mačko, čeprav je v tem času bolje, da ne začnete nove živali. Mačji pesek bi moral menjavati pogosteje in po možnosti nekdo drug. Hraniti ga je treba samo s kuhanim ali konzerviranim mesom.
3. Svežo zelenjavo je treba pred zaužitjem dobro oprati, da onesnažena zemlja ne pride v hrano.
4. Po vrtnarjenju si temeljito umijte roke, še posebej pred jedjo.
Med akutno toksoplazmozo pri nosečnici in pojavom nalezljivega procesa pri plodu mine veliko časa. Če se okužba razvije v prvi polovici nosečnosti, se lahko zastavi vprašanje induciranega splava, saj se tveganje za prenos na plod v zgodnjih fazah približa 20 %, posledice pa so uničujoče. V poznih fazah nosečnosti se nosečnica zdravi s pirimetaminom, sulfonamidi, tindurinom. Uspešno se uporablja makrolidni antibiotik spiromicin.
klamidija
Klamidije se najpogosteje prenašajo spolno in prizadenejo predvsem celice valjastega epitelija. Dokazano je tudi
možnost širjenja klamidije na "domači" način, predvsem med majhnimi otroki.
Klinične manifestacije klamidije. Vnos klamidije v genitourinarni trakt ne spremljajo vedno opazne klinične manifestacije. Bolezen je pogosto submanifestna ali asimptomatska. Polovica okuženih žensk nima kliničnih manifestacij. Klamidijski uretritis nima posebnih manifestacij, bolniki pa se redko pritožujejo zaradi disurije. Včasih lahko klamidija povzroči eksudativno vnetje kanalov in Bartholinovih žlez. Cervicitis je glavni in najpogostejši znak klamidijske aktivnosti. Izcedek iz cervikalnega kanala macerira slojevit skvamozni epitelij vaginalnega dela materničnega vratu, kar povzroči njegovo delno luščenje. Maternični vrat postane edematozen, hiperemičen, nastane tako imenovana hipertrofična ektopija materničnega vratu. Klamidijski salpingitis je najpogostejša manifestacija naraščajoče klamidijske okužbe. Značilnost klamidijskega salpingitisa in salpingooforitisa je njihov dolg, subakutni, izbrisan potek brez nagnjenosti k "teži". Kronična okužba lahko povzroči obstrukcijo jajcevodov, zunajmaternično nosečnost in neplodnost. Pri ženskah z naraščajočo klamidijsko okužbo z vnetno boleznijo medenice se lahko razvije perihepatitis, Fitz-Hugh-Ciirtisov sindrom. Za ta sindrom so značilne zvišana telesna temperatura, bolečine v jetrih in medeničnih organih.
Poleg urogenitalne klamidije je možna tudi ekstragenitalna okužba s klamidijo (oftalmoklamidija), medtem ko ima 72 % bolnikov z oftalmoklamidijo tudi klamidijsko okužbo urogenitalnega trakta.
Urogenitalna klamidija se pri nosečnicah diagnosticira v 3-12 %, doseže 33-74 % pri kroničnih vnetnih boleznih spolnih organov, kroničnih nespecifičnih pljučnih boleznih, poslabšani porodniški anamnezi (mrtvorojenost, intrauterina pljučnica pri novorojenčku, prezgodnji porod, navadni porod) .
Nosečnost s klamidijo praviloma poteka z zapleti. V prvem trimesečju je značilna grožnja prekinitve nosečnosti, nosečnost, ki se ne razvija, splavi. Pogostnost splavov je 25%, perinatalne izgube pri prezgodnjem porodu - do 5,5%.
Klamidija vodi ne le do običajnega splava, temveč tudi do intrauterine okužbe ploda in novorojenčka. Klamidija kolonizira predvsem veznico, nazofarinks, dihala, črevesje, najbolj značilna pa je lezija možganske ovojnice in možganske snovi, kjer so že makroskopsko določene usedline, podobne bombažu, predvsem na zgornjih stranskih površinah hemisfer. Histološko so videti kot granulomi. Posledica okužbe s klamidijo je povečanje antenatalne umrljivosti, pojav trahomu podobnega konjunktivitisa in pljučnice pri novorojenčkih. Ko se amnijska membrana okuži, se razvije polihidramnij, specifična lezija posteljice vodi do razvoja fetoplacentne insuficience (27%), sdfd in hipoksije ploda. Perinatalna umrljivost pri klamidiji doseže 15,5 %, delež novorojenčkov, ki so umrli v poporodnem obdobju, pa je več kot polovica vseh perinatalnih izgub.
Klinične manifestacije. Pri 17-30 % nosečnic se klamidija pojavlja latentno ali z manjšimi simptomi. V prisotnosti mešane okužbe je lahko s celotnim kompleksom simptomov, vključno z cervicitisom z ektopijo materničnega vratu.
Klamidija pri nosečnicah se običajno kombinira z bakterijsko in virusno okužbo, zato se zaradi skupnega učinka teh povzročiteljev pogosto pojavi okužba ploda. To povzroča polimorfizem kliničnih manifestacij okužbe pri novorojenčku, zato poleg tipičnih manifestacij klamidijske okužbe (konjunktivitis, vulvovaginitis, pljučnica) obstajajo oblike, ki niso značilne za klamidijo (vesikulopustuloza, omfalitis, rinitis, rinitis). .
Klinične manifestacije intrauterinih nalezljivih bolezni pri novorojenčkih, rojenih materam s klamidijo, so razdeljene v tri skupine: manjše oblike, hude oblike in tako imenovani infekcijski sindrom.
Majhne oblike vključujejo:
konjunktivitis;
Vulvovaginitis;
Vesikulopustuloze, rinitis, vnetje srednjega ušesa, omfalitis - z mešano okužbo.
Hude oblike intrauterine okužbe pri novorojenčku s klamidijsko okužbo:
klamidijska pljučnica;
Splošni vnetni proces z razvojem sepse in prisotnostjo več žarišč okužbe (pljučnica, flebitis popkovnične vene, meningitis, hepatitis) - z mešano okužbo.
Pri sindromu okužbe so lokalne in generalizirane manifestacije intrauterine okužbe odsotne. Pri novorojenčkih so motene prilagoditveni procesi, razbarvanje kože, zmanjšan mišični tonus, nestabilnost refleksov, dolgotrajna zlatenica, začetna izguba teže 10% ali več, počasno okrevanje s ponavljajočim se padcem.
Preprečevanje in zdravljenje klamidije med nosečnostjo. Zdravljenje klamidije med nosečnostjo ima določene težave, kar je povezano s posebnostmi poteka bolezni, sočasno disfunkcijo placentnega sistema, možnostjo negativnih učinkov tradicionalnih režimov zdravljenja na plod.
Antibakterijska terapija se izvaja z zdravili iz skupine makrolidov: josamicin, azitromicin. V primeru individualne intolerance na zgornja zdravila je sprejemljiva uporaba cefalosporinov III generacije.
lokalna terapija. Pri 95% bolnikov s klamidijsko okužbo so disbiotične motnje mikrobiocenoze različne resnosti, ki jih spremlja povečanje pH vaginalne vsebine na 5,9. Poleg tega imajo bolniki z urogenitalno klamidijo pogosto znatno kontaminacijo s kvasovkami iz rodu Candida. Ti rezultati kažejo na potrebo po kombinirani uporabi antibiotikov, eubiotikov in antimikotikov. Lokalna terapija vključuje saniranje nožnice, ki ji sledi predpisovanje eubiotikov peroralno in lokalno.
Imunomodulatorji in interferonski korektorji. Značilnost okužbe s klamidijo je sprememba funkcionalne aktivnosti imunskega sistema, odstopanja v ravni krožečih imunskih kompleksov, zaviranje celične imunosti, zmanjšanje fagocitne aktivnosti krvnih polinuklearnih celic in makrofagov ter zaviranje delovanje nespecifičnih obrambnih dejavnikov telesa. Za preprečevanje imunskih motenj, povezanih s klamidijo, se predpisujejo pripravki laktoflore (bifidobacteria bifidum, posušeni laktobacili,
floradophilus), ki ne le popravljajo mikrobiocenozo gastrointestinalnega trakta, ampak s stimulacijo timusno odvisnih con mezenteričnih bezgavk aktivirajo imunski odziv. Rastlinski adaptogeni imajo imunomodulatorne lastnosti, ki povečajo splošno nespecifično odpornost telesa na okužbe. Zdravilo rekombinantnega interferona se uporablja z visoko učinkovitostjo.
Preprečevanje disfunkcije fetoplacentarnega kompleksa. Za izboljšanje uteroplacentarnega krvnega obtoka se uporabljajo vazoaktivna zdravila in antiagregacije. Kot metabolično zdravljenje je predpisana dieta z visoko vsebnostjo beljakovin, fermentiranih mlečnih izdelkov ob hkratni uporabi encimskih pripravkov. Tokoferol acetat (vitamin E), hepatoprotektivna sredstva, se uporabljajo kot zdravila, ki aktivirajo presnovo.
sifilis
Prirojeni sifilis se razvije kot posledica transplacentnega širjenja Treponema pallidum od matere do ploda. Pri svežih oblikah okužbe pri materi je tveganje za okužbo ploda relativno veliko v primerjavi s tveganjem okužbe v pozni fazi bolezni. Skoraj vsi otroci, katerih matere med nosečnostjo trpijo za zgodnjim stadijem nezdravljenega sifilisa, so okuženi, stopnja umrljivosti pa je zelo visoka. Prej je veljalo, da T. pallidum začne prehajati skozi posteljico po 18-20 tednih nosečnosti, ko plast Langerhansovih celic izgine. Zdaj je dokazano, da lahko do transplacentalne okužbe ploda pride že prej, vendar zaradi imunološke nezrelosti ploda ni tipične reakcije na okužbo. Z uporabo ustreznih metod obarvanja odkrivamo spirohete v zarodkih med splavom v prvem trimesečju.
Okužba v zgodnjem fetalnem obdobju se konča z mrtvorojenjem z maceracijo in vodenico ploda. Običajno ima splav značilen videz: strnjena lobanja, štrleči trebuh, hepatosplenomegalija, vezikularne kožne lezije, sdfd. Histološko značilna areaktivna nekroza v organih s kopičenjem spirohete v obliki gnezd ali glomerulov v središčih nekrotičnih žarišč. Proliferativne spremembe niso značilne. V posteljici prevladuje žariščni vilusitis z značilnim endarteritisom glede na vrsto videza.
teracionalna angiopatija, pa tudi različne vrste nezrelosti drevesa resice.
Klinične manifestacije. Prirojeni sifilis je multisistemska bolezen, ki se zelo razlikuje po resnosti in različnih oblikah. Pojavi se pri 50 % novorojenčkov, rojenih materam s primarnim ali sekundarnim nezdravljenim sifilisom med nosečnostjo (preostalih 50 % je mrtvorojenih, zelo prezgodaj rojenih in umrlo v zgodnjem neonatalnem obdobju). Njegove manifestacije spominjajo na sekundarni sifilis.
Manifestacije prirojenega sifilisa
1. Splav ali mrtvorojenost: maceriran plod, kolabirana lobanja, štrleči trebuh, hepatosplenomegalija, hidrops fetalis, vezikularne kožne manifestacije.
2. Dropsy plod.
3. Patološko povečana posteljica (otrok je lahko normalen, očitno okužen ali mrtvorojen).
4. Prezgodnji porod.
6. Mukokutane manifestacije: vztrajen rinitis, makulopapulozni, luskasti ali bulozni izpuščaj, običajno na dlaneh in stopalih.
7. Hepatosplenomegalija, limfadenopatija.
8. Anemija, trombocitopenija
9. Zlatenica (hepatitis in/ali hemoliza).
10. Poškodbe kosti: simetrični osteohondritis, periostitis, osteomielitis dolgih kosti, lobanje, hrbtenice in reber. Pozneje se lahko razvije tipična rentgenska slika, psevdo-paraliza.
11. Poškodbe centralnega živčnega sistema, običajno asimptomatske. Na poškodbe kažejo spremembe v cerebrospinalni tekočini.
Večina živorojenih otrok je videti zdravih, nekateri imajo vezikularne bulozne lezije na dlaneh in podplatih, vendar se lahko 4 dni po rojstvu pojavijo naslednji simptomi:
1) gripi podoben sindrom:
meningealni simptomi;
solzenje (vnetje šarenice);
Izcedek iz nosu; sluznice so hiperemične, edematozne, erodirane;
Angina (na sluznici žrela so papule);
Generalizirana artralgija (zaradi bolečine ni aktivnih gibov v okončinah - Parrojeva psevdoparaliza; na rentgenskem posnetku - pojav osteohondritisa, periostitis je pogosto opažen, zlasti golenice (sabljaste noge);
2) povečanje vseh skupin bezgavk:
Cervikalni, komolec, dimeljski, aksilarni, poplitealni;
Hepatosplenomegalija (v hudih primerih - anemija, purpura, zlatenica, edem, hipoalbuminemija);
3) izpuščaji:
makulopapuloza;
Spajanje papuloznih lezij s tvorbo širokih kondilomov.
Preprečevanje. Preprečevanje prirojenega sifilisa se zmanjša na presejalni pregled nosečnic za pravočasno odkrivanje bolnikov. Ko se diagnoza postavi v prvem trimesečju nosečnosti, je indicirana njena prekinitev glede na dejstvo, da okužba v zgodnjih fazah nosečnosti povzroči nastanek hudih poškodb pri plodu. Če se sifilis odkrije v pozni nosečnosti, se zdravljenje izvaja v skladu s priporočili Ministrstva za zdravje Ruske federacije, po splošno sprejetih shemah, odvisno od stopnje poteka bolezni.
Če se sumi ali potrdi prirojeni sifilis, je treba novorojenčka izolirati do uvedbe specifične terapije in dodatnih 24 ur od njenega začetka.
Zdravljenje. Posebno zdravljenje se izvaja pri novorojenčkih v naslednjih kliničnih situacijah:
Če je bilo zdravljenje matere neustrezno;
Če je bila opravljena v zadnjih 4 tednih nosečnosti;
Če se o njem nič ne ve;
Če so bila za zdravljenje uporabljena druga zdravila kot penicilin.
Poleg tega se upoštevajo rezultati reaginskih testov. Višji titer protiteles kot pri materi kaže na aktiven infekcijski proces. Titer protiteles je treba sčasoma spremljati, saj lahko kaže le na transplacentalni prenos materinih protiteles na plod. Če se titer protiteles zmanjša v prvih 8 mesecih življenja, se pri novorojenčku ne
okužen. S pozitivnim rezultatom testa se zdravljenje izvaja v tistih opazovanjih, ko ni mogoče sčasoma nadzorovati titrov protiteles.
Izbirno zdravilo za zdravljenje prirojenega sifilisa je penicilin G (prokainpenicilin, benzatinpenicilin). Dnevni odmerek zdravila se izračuna glede na telesno težo novorojenčka in njegovo starost.
Spremljanje učinkovitosti zdravljenja se izvaja glede na rezultate kvantitativnih netreponemskih testov, ki se izvajajo pri starosti 3, 6 in 12 mesecev. Negativni rezultat testa kaže na učinkovitost zdravljenja. Ohranjanje in povečanje titra protiteles zahteva nadaljnji pregled in ponovno zdravljenje.
Virusni hepatitis
Akutni virusni hepatitis lahko povzroči vsaj pet različnih povzročiteljev, vendar se okužbe jeter, ki jih povzroča Epstein-Barr virus, citomegalovirus in virus rumene mrzlice, obravnavajo kot ločene bolezni in običajno niso vključene v izraz "akutni virusni hepatitis".
dodeli:
virusni hepatitis A;
virusni hepatitis B;
Virusni hepatitis, ne A niti B (sporadični in epidemijski), vključno s hepatitisom C (HCV);
Virusni hepatitis D (hkratna okužba s hepatitisom B - sočasna okužba in zaporedna okužba s hepatitisom B - superinfekcija).
Virus hepatitisa A (HAV) spada v rod enterovirusov družine pikornovirusov. Virus, ki vsebuje RNA, je sestavljen iz viriona brez ovoja.
Najbolj raziskan je virus hepatitisa B (HBV). Spada med hepadnoviruse in ima bolj zapleteno strukturo kot virus hepatitisa A. Infekcijski delec je sestavljen iz jedra (skorje) in zunanje lupine (kapsida). Sestava viriona vključuje krožno dvojno verigo DNA in DNK polimerazo; replikacija virusnih delcev se pojavi v jedrih okuženih hepatocitov.
Vsaj štirje različni sistemi antigen-protitelo so povezani z virusom hepatitisa B.
1. Surface AG (HBsAg, Australian AG) je povezan z beljakovinsko prevleko virusa. Njegovo odkrivanje v krvni plazmi omogoča diagnosticiranje akutnega hepatitisa B in pomeni, da je pacientova kri postala potencialni vir okužbe. HBsAg se odkrije v inkubacijskem obdobju (1-6 tednov pred razvojem kliničnih in biokemičnih znakov bolezni) in izgine po okrevanju. Ustrezna protitelesa (anti-HBs) je mogoče odkriti, kar pomeni, da kasneje, tedne ali mesece po kliničnem okrevanju, njihova prisotnost kaže na preteklo okužbo in relativno zaščito v prihodnosti. V 10 % se HBsAg še naprej odkrije po akutni fazi in se ustrezna protitelesa ne pojavijo - pri takih bolnikih se običajno razvije kronični hepatitis ali postanejo asimptomatski nosilci virusa.
2. Core AG (HBcAg) je povezan z jedrom (core) viriona. Najdemo ga v okuženih jetrnih celicah, v plazmi pa ga zaznamo le, če s posebnimi tehnikami uničimo virusne delce. Ustrezna protitelesa (anti-HBc) se običajno odkrijejo na začetku obdobja manifestacije; nato se njihov titer postopoma zmanjšuje. Prisotnost AT-HBc skupaj z AT-HBs kaže na predhodno okužbo.
3. Antigen e (HBeAg) je očitno peptid, ki je del virusnega jedra. Najdemo ga samo v HBsAg-pozitivni plazmi. Prisotnost kaže na aktivno razmnoževanje virusa in je združena s povečano infekcijsko sposobnostjo krvi in verjetnostjo razvoja kronične okvare jeter.
Virus hepatitisa D (HDV, delta faktor) je edinstven. Njegova RNA je okvarjena, zaradi česar se ta virus lahko razmnožuje le v prisotnosti HBV. Hepatitis D se pojavi bodisi kot sočasna okužba pri akutnem hepatitisu B ali kot superinfekcija pri izrazito kroničnem hepatitisu B. Okuženi hepatociti vsebujejo delta delta, prevlečene s HBsAg. Klinično se okužba kaže z nenavadno hudim potekom akutnega hepatitisa B.
Predlagano je, da se izraz ne-A ne-B hepatitis (NANB) nanaša na okužbe, ki niso povezane z virusi tipa A in B. Relativno nedavno je bil identificiran specifičen enoverižni RNA virus, podoben flavivirusom (virus hepatitisa C), ki je
povzročajo večino potransfuzijskih in sporadičnih primerov NANB hepatitisa. Značilnost HCV je izjemno visoka heterogenost njegovega genoma. Ugotovljenih je bilo vsaj šest glavnih genotipov virusa. Protitelesa proti HCV se pogosto pojavijo v plazmi nekaj mesecev po akutni okužbi. Titri se nato postopoma znižujejo, razen če okužba postane kronična (kar je v 50 %). Virus HCV se identificira v plazmi s kompleksno tehniko, ustrezen antigen je izoliran iz hepatocitov.
Virus hepatitis Aširi se predvsem po fekalno-oralni poti, možna je tudi okužba s krvjo in produkti izločanja. Vir okužbe je le bolnik v zgodnji fazi bolezni – izključeni so nosilci virusov in kronične oblike okužbe. Za prodromalno (preikterično) stopnjo so značilna akutna vročina, mrzlica, glavobol in dispeptične motnje. V tej fazi se pogosto opazi srbenje, ki ga spremlja povečanje velikosti jeter, povečanje ravni transferaz v krvi 5-7 dni pred pojavom zlatenice. Pogosto je okužba asimptomatska.
Virus hepatitis B običajno se prenaša parenteralno: preko okužene krvi in njenih derivatov. Možna okužba med tetoviranjem. Prenos med odvisniki od drog ostaja visok, tveganje za bolnike na hemodializi in bolnišnično osebje, ki pride v stik s krvjo, pa je povečano. Obstaja neparenteralno spolno širjenje. Kronični prenašalci HBV služijo kot rezervoar okužbe.
Okužbo s HBV spremlja širok spekter lezij jeter, od subkliničnega prenosa do akutnega in kroničnega hepatitisa, ciroze in hepatocelularnega karcinoma. Po dolgi inkubacijski dobi (6 tednov do 6 mesecev) se pojavijo znaki akutne okužbe. Predikterično obdobje v nasprotju s hepatitisom A traja dlje in je značilno postopno nastopanje z artralgijo, urtikarskim izpuščajem, dispeptičnih in asteničnih motenj, narašča hepatolienalni sindrom. Pri hudih oblikah bolezni se temperatura dvigne. V krvi - povišane vrednosti transaminaz; HBsAg, HBeAg in
S pojavom zlatenice se poveča zastrupitev, dispeptične, astenične manifestacije in še bolj - hepatolienalni sindrom.
Potek zlatenice je bolj izrazit. V hudih primerih se lahko razvije hemoragični sindrom, akutna jetrna encefalopatija s prehodom v komo in celo smrt.
Pri nosečnicah s hepatitisom B je visoka incidenca prezgodnjih porodov in preeklampsije. Več kot 50 % žensk ima vnetne spremembe v porodu.
Hepatitis ali Ani B(NANB) ima različico, podobno hepatitisu A, ki se večinoma širi z izbruhi, ki se prenašajo z vodo. Različica, ki je blizu hepatitisu B, običajno s krajšo inkubacijsko dobo, pogosto vodi v nastanek kroničnega hepatitisa.
Končno obstajajo mešane različice okužbe (A in B, B in D, B in CMV, B in HIV).
Povprečno trajanje inkubacijske dobe za okužbo s hepatitisom A je 2-6 tednov, hepatitis B - 6-25 tednov, niti A niti B - 2-25 tednov. Otroci in mladostniki so pogosteje prizadeti, vendar se bolezen lahko pojavi v kateri koli starosti.
Virusni hepatitis je najpogostejši vzrok zlatenice med nosečnostjo. Običajno poteka razmeroma lahko, vendar ob podhranjenosti ne more nastopiti huda epidemijska oblika hepatitisa, ne A niti B. Umrljivost mater je 0,64-1,79 %, lahko pa doseže 15,6 % (Farber N.A. et al., 1990). Hepatitis je hujši v drugi polovici nosečnosti, kar je povezano s spremembami hormonske ravni, izrazitejšimi simptomi holestaze.
Prirojeni virusni hepatitis se pojavi redko, z akutnim ali kroničnim hepatitisom B matere med nosečnostjo; Tudi mati z asimptomatsko obliko hepatitisa (nosilec antigena) je lahko vir intrauterine okužbe. Za fetalni hepatitis je značilen polimorfizem hepatocitov s tvorbo multinuklearnih celic simplasta, pa tudi holestaza (intracelularna in intratubularna), nastanek adenomatoznih struktur in žolčna nekroza s slabo limfocitno infiltracijo portalnih poti. Hud hepatitis pri materi lahko povzroči prenatalno smrt ploda. Makroskopsko se v porodu opazi rumenkasta barva membran, plodna površina posteljice, histološko, pri spontanih splavih, so v stromi resic posteljice in membrane, ki absorbirajo bilirubin, zabeležene številne Kashchenko-Hofbauerjeve celice. minimalne vnetne spremembe.
Prepričljivi podatki o teratogenosti hepatitisa v prvem trimesečju nosečnosti niso na voljo. Virus hepatitisa B se lahko prenese na novorojenčka ob rojstvu ali, redkeje, skozi posteljico. V I in II trimesečju nosečnosti se akutni hepatitis B redko prenaša na plod (5 %). Prenos s placente ni dokončno ugotovljen in je najverjetneje pri e-antigen pozitivnih materah, ki so kronične prenašalke površinske hipertenzije hepatitisa B (HBsAg) ali pri katerih se je hepatitis B razvil v tretjem trimesečju. Z boleznijo v III trimesečju je verjetnost okužbe ploda 60-70%. Najpogosteje pride do okužbe med porodom zaradi mikrotransfuzije krvi od matere do ploda ali kot posledica stika otroka z okuženimi izločki matere pri prehodu skozi porodni kanal. Pozitiven test HBeAg (ki odraža visoko stopnjo okužbe) je povezan z 80-90 % možnostjo prenosa na plod. Več kot 85% novorojenčkov takšnih mater postane kronični nosilci. Če ima mati protitelesa proti HBeAg (njihova prisotnost kaže na odpravo okužbe), je tveganje za okužbo le 25 %. Možna okužba v poporodnem obdobju (z mlekom, slino)
Okuženi novorojenčki pogosto postanejo nosilci HBV in imajo subklinično jetrno disfunkcijo. Opažanja očitnega neonatalnega hepatitisa so redka.
Napoved. Hepatitis A običajno spontano izzveni v 4 do 8 tednih – v večini primerov ne zahteva posebnega zdravljenja. Omejitev prehrane in telesne dejavnosti ni potrebna. Pogostost splavov ne presega tiste v populaciji. Zarodek praktično ni izpostavljen tveganju okužbe in novorojenček ne potrebuje profilakse.
Pri hepatitisu B je napoved manj ugodna kot pri A. Še posebej po transfuziji krvi, ko lahko umrljivost doseže 10-15 %; pri 5-10% nastane kronična oblika. Smrtnost pri nosečnicah je 3-krat višja kot pri nenosečih ženskah. Incidenca hepatitisa pri novorojenčkih je 45-62%.
Največja nevarnost za nosečnice je epidemijska varianta hepatitisa NANB v II in III trimesečju nosečnosti. Zapleti: spontani splavi, prezgodnji porodi, visoka umrljivost mater, neonatalna obolevnost in perinatalna umrljivost.
Preprečevanje in zdravljenje okužb. Osebna higiena pomaga preprečevati hepatitis A. Če pride nosečnica v stik z bolno osebo 7-10 dni, je standard γ -globulin 1,5-3,0 ml enkrat intramuskularno. Kasneje je uporaba zdravila nepraktična.
Za preprečevanje hepatitisa B je treba uvesti omejitve transfuzije, uvesti uporabo krvi, testirane na HBsAg. Potreben je pregled darovalca za HCVAg. Standardni imunoglobulin zagotavlja zaščito pred klinično okužbo s HAV in se daje tistim, ki imajo gospodinjske stike z uveljavljenim nosilcem.
Cepljenje proti HBV vodi do tvorbe protiteles pri zdravih prejemnikih in zmanjša razširjenost hepatitisa za 90 %. Bolniki na dializi, s cirozo jeter in drugimi imunskimi motnjami se slabše odzivajo na cepljenje. Majhen delež zdravih ljudi se ne odzove s tvorbo AT-HB.
Pregled nosečnic na nosilnost HBsAg je treba opraviti že v zgodnji nosečnosti.
Pri hepatitisu C vloga perinatalne okužbe pri širjenju te okužbe ni v celoti določena. Odkrivanje RNA virusa hepatitisa C v krvnih serumih otrok 1.-5. dan po rojstvu daje razumno domnevo, da je pri tej okužbi prisotna tudi prenatalna okužba. Zdravljenje hepatitisa C temelji na terapiji z interferonom (interferon, induktorji interferona), pa tudi z uporabo protivirusnih zdravil.
Z blagim in zmernim hepatitisom (kateri koli) v prvem trimesečju nosečnosti se lahko nosečnost nadaljuje, saj bo ženska do poroda zdrava in verjetnost prirojenih anomalij pri njenem otroku ni večja kot pri zdravem. Pri hudem hepatitisu po okrevanju, odvisno od značilnosti poteka okužbe in trajanja nosečnosti, ga je priporočljivo prekiniti: do 12 tednov - medicinski splav, po 12 tednih - intraamnialno dajanje hipertonične raztopine natrijevega klorida, prostaglandina F2a ; intramuskularno z uvedbo prostaglandina po predhodni (12-urni) razširitvi materničnega vratu s srednje velikimi algami.
Pri zdravljenju fizični počitek, uravnoteženo pitje, zdravljenje grožnje prezgodnje prekinitve nosečnosti in po možnosti premik v času fiziološkega poroda, ki sredi zlatenice ne nosijo le neželenega fizičnega napora, ampak tudi nenadne hormonske pomembne so spremembe, ki lahko pripeljejo telo iz kompenziranega relativnega ravnovesja. Prikazana previdna infuzijska detoksikacijska terapija pod nadzorom diureze. Pri zastajanju tekočine se uporabljajo diuretiki. Kratek tečaj glukokortikoidov - kot sestavni del sklopa ukrepov za dehidracijo pri razvoju možganskega edema. Imenovanje kortikosteroidne terapije je nepraktično in lahko celo prispeva k rasti hepatocitodistrofije.
Otroci, rojeni HBsAg-pozitivni materi, ne glede na to, ali ima serumski antigen HBe ali protitelesa, bi morali nemudoma po rojstvu prejeti profilaktično zdravljenje z imunoglobulinom proti hepatitisu B (HBIg), nato pa bi morali prejeti tri cepljenja z rekombinantnim cepivom proti hepatitisu C. Izolacija novorojenčkov od mater in zavrnitev dojenja ni priporočljiva, še posebej po uvedbi HBIg in protivirusnega cepiva. Če se HBsAg izloča v materino mleko, da se prepreči okužba v obdobju novorojenčka, dojenje ni indicirano.
Zdravljenje novorojenčkov z akutnim hepatitisom B je simptomatsko z ustrezno prehrano; niti steroidi niti HBIg niso učinkoviti. Okuženega novorojenčka je treba izolirati in pri delu z njegovo krvjo in drekom biti izjemno previdni.
PRIPRAVA NA NOSEČNOST IN VODENJE NOSEČNOSTI
Tako intrauterine okužbe resno ogrožajo življenje in zdravje ploda in novorojenčka ter imajo pogosto škodljive dolgoročne posledice. Diagnoza in zdravljenje nalezljivih bolezni pri nosečnicah predstavljata velike težave zaradi zamegljenosti, raznolikosti in nespecifičnosti kliničnih manifestacij, težav pri pridobivanju materiala za laboratorijske preiskave in nezmožnosti široke uporabe terapevtskih zdravil.
V zvezi z navedenim so posebnega pomena preventivne metode IUI, ki temeljijo na preprečevanju in zdravljenju okužbe pri materi. Najbolj obetavna v tej smeri je predporodna priprava zakonskih parov, ki ji sledi dosledno izvajanje medicinskih in diagnostičnih ukrepov med nosečnostjo.
Priprava pred gravidom mora vključevati:
Identifikacija rizične skupine na podlagi anamneznih podatkov in rezultatov kliničnega pregleda, ugotavljanje spremljajočih ekstragenitalnih bolezni;
Celovit pregled s preučevanjem imunskega, hormonskega, mikrobiološkega stanja;
Etiotropno antibakterijsko ali protivirusno zdravljenje;
Izvedba ustrezne korekcije ugotovljenih kršitev mikrocenoze genitalnega trakta, ki ji sledi imenovanje eubiotikov;
Zdravljenje bolezni z uporabo imunostimulirajoče in interferonske terapije ter fizioterapije;
metabolična terapija;
Odpravljanje menstrualnih nepravilnosti in povezanih endokrinopatij;
Zdravljenje spolnega partnerja ob prisotnosti spolno prenosljivih bolezni.
Med nosečnostjo v terminih do 12, pa tudi pri 18-20, 28-30 in 37-38 tednih pri nosečnicah te skupine je prikazana ocena stanja vaginalne mikrocenoze do 12 tednov (nadalje glede na indikacije pri 18-20 in 37-38 tednih) - identifikacija povzročiteljev spolno prenosljivih bolezni in določitev titra specifičnega Ig proti virusnim in bakterijskim povzročiteljem. Ko se odkrijejo okužbe, se izvede ustrezno zdravljenje, ki je izbrano ob upoštevanju trajanja nosečnosti in možnega učinka zdravil na razvoj ploda.
Redni ehografski, doplerometrični in kardiotokografski pregledi omogočajo pravočasno diagnozo razvoja fetoplacentarne insuficience, zdravljenje in spremljanje njene učinkovitosti.
Izvajanje predporodne priprave in ukrepov za ugotavljanje ogroženih intrauterinih okužb
omogoča zmanjšanje pogostosti intrauterinih okužb za 2,4-krat. Hkrati se zmanjša število zapletov nosečnosti in poroda (zlasti prezgodnja prekinitev nosečnosti, pa tudi fetoplacentna insuficienca), kar pomaga zmanjšati splošno pojavnost novorojenčkov za 1,5-krat.
Intrauterina okužba ima lahko različne manifestacije, odvisno od tega, kako dolgo je prišlo do okužbe ploda.
- 3-12. teden nosečnosti: prekinitev nosečnosti (splav) ali nastanek malformacij ploda (odstopanja od normalne strukture telesa, ki se pojavijo med intrauterinim ali redkeje poporodnim razvojem);
- 11-28 teden nosečnosti: pride do intrauterine zastoja v rasti, otrok se rodi z nizko telesno težo, malformacijami ploda (na primer nepravilnosti v razvoju srca (nepravilna tvorba predelnih sten itd.)).
- 10-40 tednov nosečnosti: fetopatija (bolezni ploda; poškodbe plodovih organov, na primer fetalna pljučnica (nastane pljučnica pri plodu).
Če spontanega splava (splava) ni bilo in je bil otrok rojen z okužbo v predporodnem obdobju, imajo takšni otroci (v različnih stopnjah resnosti in v eni ali drugi kombinaciji) naslednje znake:
- intrauterino zaostajanje v rasti;
- hepatosplenomegalija (povečanje jeter in vranice);
- zgodnja zlatenica;
- izpuščaj drugačne narave;
- motnje dihalne funkcije;
- srčno-žilna insuficienca;
- nevrološke motnje;
- visoka telesna temperatura v prvem dnevu življenja;
- vnetne (npr. konjunktivitis) in degenerativne (npr. atrofija vidnega živca) očesne bolezni.
Takšni otroci se rodijo brez znakov motenj, vendar se čez nekaj časa (najpozneje tretji dan življenja) pojavijo:
- letargija;
- bledica;
- izguba apetita;
- povečana regurgitacija;
- odpoved dihanja;
- poškodba katerega koli organa (z okužbo med porodom se vnetje opazi pogosteje kot en organ, na primer pljuča, jetra itd.).
Vzroki
- Okužba ploda prihaja od bolne matere.
- Mehanizmi okužbe:
- transplacentalna (hematogena) pot - povzročitelj iz matere vstopi v plod skozi posteljico (na ta način se pogosto prenašajo virusi in toksoplazma);
- naraščajoča pot - pot okužbe, pri kateri okužba iz genitalnega trakta vstopi v maternično votlino in nato lahko okuži plod (značilno za okužbo s klamidijo, enterokoki);
- padajoča pot - patogen iz jajcevodov se vnese v maternično votlino, nato pa v telo ploda;
- kontaktna (intranatalna) pot - okužba ploda se pojavi med prehodom skozi porodni kanal, na primer pri zaužitju okužene amnijske tekočine, ko povzročitelj iz okužene amnijske tekočine vstopi v sluznice in oči.
- Dejavniki, ki prispevajo k razvoju intrauterine okužbe ploda:
- bolezni genitourinarnega sistema pri materi (erozija materničnega vratu, okužba v obliki uretritisa (vnetje sečnice), cistitis (vnetje mehurja), pielonefritis (vnetna bolezen ledvic) itd.);
- okužbe, prenesene med nosečnostjo, tudi SARS (akutna respiratorna virusna okužba);
- stanja imunske pomanjkljivosti, vključno z okužbo s HIV;
- stanja po presaditvi organov in tkiv.
Diagnostika
- Diagnoza intrauterine okužbe med nosečnostjo je težka, saj intrauterino okužbo ploda ne spremljajo nobene posebne manifestacije pri materi.
- V fazi načrtovanja nosečnosti spolno prenosljive bolezni in najpogostejše urogenitalne okužbe diagnosticiramo s PCR (polimerazno verižno reakcijo). Med nosečnostjo se izvaja tudi diagnostika prisotnosti teh bolezni, saj je imuniteta nosečnice fiziološko zmanjšana, oziroma se poveča dovzetnost za različne nalezljive bolezni.
- Diagnoza krvi nosečnice za okužbo s TORCH, HIV, sifilis (venerična bolezen, ki prizadene kožo, sluznice, notranje organe, kosti, živčni sistem), hepatitis B in C s preiskavo krvi na prisotnost protiteles (zaščitnih teles) proti povzročitelji teh okužb.
- Sestavo in količino zaščitnih teles (imunoglobulinov) M in G lahko uporabimo tudi za presojo tveganja za intrauterino okužbo ploda:
- odkrivanje specifičnega IgG v majhni količini kaže, da je bila okužba v preteklosti, da je bila oblikovana imunost proti temu patogenu in bolezen ne predstavlja nevarnosti niti za mater niti za otroka;
- povečanje vsebnosti IgG ali pojav IgM kaže na ponovni pojav okužbe. Verjetnost intrauterine okužbe je relativno majhna;
- na vrhuncu okužbe pri ženski, ki prej ni bila bolna z eno ali drugo boleznijo, se odkrije le IgM. Pri nekaterih okužbah (na primer pri okužbi s herpesvirusom ali citomegalovirusom) je tveganje za okužbo ploda med začetno okužbo nosečnice približno polovica primerov.
- Ultrazvočni pregled za diagnosticiranje delovanja posteljice, krvnega pretoka ploda (spremembe v strukturi posteljice, na primer njena odebelitev, povečana ali zmanjšana vsebnost plodovnice, prisotnost suspenzije v plodovnici lahko kaže na prisotnost intrauterine okužba ploda).
- V nekaterih primerih je predpisana biopsija horiona (odvzem dela zunanje lupine zarodka za študijo), sledi amniocenteza (vzorčenje amnijske tekočine), kordocenteza (pregled popkovnične krvi ploda). z bakteriološko preiskavo (setev na hranilni medij z nadaljnjo oceno zraslih kolonij) na prisotnost patogena.
- Pregled posteljice (posteljice, membran in popkovine) z bakteriološkimi in imunohistokemičnimi metodami (metoda mikroskopskega pregleda tkiv na prisotnost določenega patogena).
- Serološke študije krvi novorojenčka z encimskim imunskim testom (ELISA) za določitev protiteles IgM, IgG, IgA (IgG v krvi otroka lahko kaže na vnos materinih protiteles, zato se kri novorojenčka ponovno pregleda po 3- 4 tedne; povečanje vsebnosti IgG za 4-krat ali več kaže na možen infekcijski proces.IgM v krvi novorojenčka kaže na prisotnost aktivne okužbe pri otroku).
- Otrokom s sumom na intrauterino okužbo je predpisan ultrazvok trebušne votline za odkrivanje povečanih jeter in vranice, nevrosonografija (metoda za oceno stanja struktur centralnega živčnega sistema).
- Možno je tudi posvetovanje.
Zdravljenje intrauterine okužbe
Zdravljenje je odvisno od patogena. Imenovati:
- antibakterijska zdravila;
- protivirusna zdravila;
- imunostimulirajoča zdravila;
- krepilna zdravila;
- simptomatska (odvisno od simptomov in prizadetih organov) zdravila.
Zapleti in posledice
- Spontana prekinitev nosečnosti (splav).
- Prirojene malformacije ploda (še posebej, če pride do okužbe ploda v prvih 2 mesecih njegovega razvoja).
- Zgodnja smrt novorojenčka (v prvih 1-7 dneh življenja).
- Mrtvorojenost.
- Dolgoročne posledice (na primer motnje v razvoju katerega koli organa, možganske ciste itd.).
- razvoj prirojene imunske pomanjkljivosti.
- Za druge okužbe, pridobljene pozneje pri otrocih z intrauterino okužbo, je značilen hud potek, hude poškodbe različnih organov in sistemov. Možno:
- infekcijski proces pri novorojenčku (če je stik z okužbo pri plodu prišlo tik pred porodom, se lahko otrok rodi s pljučnico (pljučnico), enterokolitisom (vnetje tankega in debelega črevesa), meningitisom (vnetje možganskih ovojnic) itd.);
- razvoj prenosa povzročitelja okužbe s tveganjem za razvoj bolezni v prihodnosti. Bakterionosilec je stanje, pri katerem je v telesu patogen, vendar ni kliničnih znakov bolezni;
- če otrok zboli že dolgo pred rojstvom, se lahko rodi zdrav, vendar z nizko telesno težo (manj kot 2500 gramov).
Preprečevanje intrauterine okužbe
V fazi načrtovanja nosečnosti in med nosečnostjo:
- diagnoza bodoče matere za prisotnost spolno prenosljivih bolezni;
- krvni test za prisotnost protiteles (zaščitnih teles) proti povzročiteljem infekcijskega kompleksa TORCH (na primer, če se med pregledom izkaže, da ženska ni imela rdečk, potem pri načrtovanju nosečnosti (vsaj 6 mesecev vnaprej) , je treba biti cepljen), HIV, sifilis (venerična bolezen, ki prizadene kožo, sluznice, notranje organe, kosti, živčni sistem) ter hepatitis B in C;
- izogibajte se stiku z bolnimi sorodniki;
- pregledati hišne ljubljenčke (na primer mačke za prisotnost toksoplazmoze);
- ne jejte hitre hrane, polizdelkov, jejte samo dobro ocvrto meso in ribe, opustite se eksotični kuhinji;
- redni obiski med nosečnostjo (1-krat na mesec v 1. trimesečju, 1-krat na 2-3 tedne v 2. trimesečju, 1-krat na 7-10 dni v 3. trimesečju);
- pravočasna prijava nosečnice v predporodno ambulanto (do 12 tednov nosečnosti);
- pravočasna priprava na nosečnost in njeno načrtovanje (pravočasno cepljenje, na primer proti rdečkam, odkrivanje in zdravljenje bolezni genitourinarnega sistema itd.);
- pravočasno in zadostno zdravljenje nalezljivih in vnetnih bolezni ženskega reproduktivnega sistema.
Poleg tega
- Najnevarnejši patogeni, ki skoraj vedno povzročajo nastanek hude patologije ploda, so okužbe, združene v tako imenovani TORCH kompleks:
- To (Toxoplasma gondii) - toksoplazmoza;
- R (virus rdečk) - rdečke;
- C (CMV) - citomegalovirus;
- H (herpes virus) - herpes.
- Spolno prenosljive bolezni (klamidija, okužbe z mikoplazmo, trihomonijaza, gonoreja) lahko povzročijo tudi patologije ploda.
- Sifilis je še posebej nevaren za plod.